بیماری دژنراتیو دیسک اصطلاحی کلی برای بیماری است که در آن دیسک بین مهره ای آسیب دیده باعث درد مزمن می شود ، که می تواند کمردرد در ستون فقرات کمر یا گردن درد در ستون فقرات گردنی باشد. به خودی خود یک "بیماری" نیست ، بلکه در واقع تجزیه دیسک بین مهره ای ستون فقرات است. دیسک بین مهره ای ساختاری است که اخیراً به دلیل پیامدهای بالینی آن بسیار مورد توجه قرار گرفته است. تغییرات پاتولوژیک که می تواند در تحلیل رفتن دیسک رخ دهد شامل فیبروز ، باریک شدن و خشک شدن دیسک است. نقص های مختلف آناتومیکی نیز می تواند در دیسک بین مهره ای مانند اسکلروز صفحات انتهایی ، شکاف و تخریب مخاطی آنولوس و تشکیل استئوفیت ها رخ دهد.
کمردرد و درد گردن از مشکلات عمده اپیدمیولوژیک است که تصور می شود مربوط به تغییرات دژنراتیو دیسک است. کمردرد دومین علت اصلی مراجعه به پزشک پزشک در آمریکا است. تخمین زده می شود که حدود 80٪ از بزرگسالان آمریکایی حداقل یک بار در طول زندگی خود از کمردرد رنج می برند. (مودیچ ، مایکل تی. ، و جفری س. راس) بنابراین ، درک کاملی از بیماری دیسک دژنراتیو برای مدیریت این بیماری مشترک لازم است.
فهرست
آناتومی ساختارهای مرتبط
آناتومی ستون فقرات
ستون فقرات ساختار اصلی است که وضعیت بدن را حفظ می کند و مشکلات مختلفی را در فرآیندهای بیماری ایجاد می کند. ستون فقرات از هفت مهره گردن رحم ، دوازده مهره سینه ، پنج مهره کمر و مهره های ساکرال و کوکسیژئال تلفیقی تشکیل شده است. پایداری ستون فقرات توسط سه ستون حفظ می شود.
ستون قدامی توسط رباط طولی قدامی و قسمت قدامی بدن مهره تشکیل می شود. ستون میانی توسط قسمت خلفی بدن مهره و رباط طولی خلفی تشکیل می شود. ستون خلفی از یک قوس بدن خلفی تشکیل شده است که دارای فرایندهای عرضی ، لایه ها ، وجوه و فرایندهای چرخشی است. (e بیماری دیژنرژن دیسک: زمینه ، آناتومی ، پاتوفیزیولوژی )
آناتومی دیسک بین مهره ای
دیسک بین مهره ای بین دو بدن مهره مجاور در ستون مهره قرار دارد. حدود یک چهارم از کل طول ستون فقرات توسط دیسک های بین مهره ای شکل می گیرد. این دیسک مفصل فیبروکارتلیاژینوز را تشکیل می دهد که به آن مفصل سمفیز نیز گفته می شود. این اجازه می دهد تا حرکت جزئی در مهره ها داشته باشد و مهره ها را در هم نگه دارد. دیسک بین مهره ای با مقاومت در برابر تنش و ویژگی های مقاومت در برابر فشرده سازی مشخص می شود. یک دیسک بین مهره ای عمدتا از سه قسمت تشکیل شده است. پلاتوز هسته هسته ژلاتینی ، فیبروز آنولوس بیرونی و غضروف های غضروفی که به طور برتر و تحتانی در محل اتصال بدن مهره ها قرار دارند.
Nucleus pulposus قسمت داخلی ژلاتین است. این پروتئین شامل ژل پروتئوگلیکان و ژل آب است که توسط کلاژن نوع II کلاژن و الیاف الاستین که بصورت شل و نامنظم مرتب شده اند ، نگه داشته می شوند. Aggrecan پروتئوگلیکان اصلی است که در هسته پالپوس یافت می شود. این تقریباً 70٪ هسته پالپوس و تقریبا 25٪ فیبروز آنولوس را تشکیل می دهد. این می تواند آب را حفظ کرده و خواص اسمزی را که برای مقاومت در برابر فشرده سازی و عمل به عنوان کمک فنر لازم دارند فراهم می کند. این مقدار زیاد آگرکان در یک دیسک نرمال به بافت اجازه می دهد تا از ریزش فشاری پشتیبانی کند و بارها به همان اندازه در فیبروز حلقوی و مهره ها در حین حرکت ستون فقرات توزیع شود. (واتر ، پل آر و همکاران)
قسمت بیرونی آنبولار فیبروز نامیده می شود ، که دارای الیاف کلاژن نوع I فراوان است که به عنوان یک لایه دایره تنظیم شده است. الیاف کلاژن به صورت خمیده بین لاملهای حلقوی در جهات متناوب اجرا می شوند و به آن توانایی مقاومت در برابر استحکام کششی را می دهند. لیگامانهای دورگرد ، فیبروز حلقوی را به صورت محیطی تقویت می کنند. از نظر قدامي ، رباط ضخيمي فيبروز آنولوس را تقويت مي کند و رباط نازک تري قسمت خلفي را تقويت مي کند. (چوی ، یونگ سو)
معمولاً بین هر جفت مهره یک دیسک وجود دارد به جز بین اطلس و محور که مهره های گردن رحم اول و دوم در بدن هستند. این دیسک ها می توانند حدود 6 حرکت کنند؟ در تمام محورهای حرکت و چرخش در اطراف هر محور. اما این آزادی حرکت بین قسمتهای مختلف ستون مهره متفاوت است. مهره های گردنی بیشترین دامنه حرکت را دارند زیرا دیسک های بین مهره ای بزرگتر هستند و یک سطح مقعر پایین و محدب فوقانی بدن مهره ای وجود دارد. آنها همچنین دارای اتصالات وجهی به طور عرضی هستند. مهره های قفسه سینه حداقل دامنه حرکتی را در خم شدن ، کشش و چرخش دارند ، اما هنگام اتصال به قفس دنده دارای خمش جانبی آزاد هستند. باز هم مهره های کمر از انعطاف و کشش خوبی برخوردار هستند ، زیرا دیسک های بین مهره ای آنها بزرگ است و فرایندهای چرخشی به صورت خلفی قرار دارند. با این حال ، چرخش کمری جانبی محدود است زیرا مفاصل وجهی به صورت ساژیتال قرار دارند. (بیماری دیسک تخریب: زمینه ، آناتومی ، پاتوفیزیولوژی)
تامین خون
دیسک بین مهره ای یکی از بزرگترین ساختارهای عروقی در بدن است که مویرگها در صفحات انتهایی ختم می شوند. بافت ها مواد مغذی را از عروق موجود در استخوان زیر غضروفی که در مجاورت غضروف هیالین در صفحه انتهایی قرار دارند ، بدست می آورند. این مواد مغذی مانند اکسیژن و گلوکز از طریق انتشار ساده به دیسک بین مهره ای منتقل می شوند. (Disc دیسک بین مهره ای ستون فقرات Orthobullets.Com )
تامین عصب
عصب دهی حسی دیسک های بین مهره ای پیچیده است و با توجه به موقعیت در ستون فقرات متفاوت است. تصور می شود انتقال حسی توسط مواد P ، کلسی تونین ، VIP و CPON صورت می گیرد. عصب مهره ای سینو ، که از گانگلیون ریشه پشتی به وجود می آید ، رشته های سطحی حلقوی را عصب کشی می کند. الیاف عصبی فراتر از الیاف سطحی نیستند.
دیسکهای بین مهره ای کمری علاوه بر این در جنبه خلفی با شاخه هایی از رامی اولیه شکمی و از رکن خاکستری رامی خاکستری در نزدیکی محل اتصال خود با رامی اولیه شکمی تأمین می شود. جنبه های جانبی دیسک توسط شعباتی از ارتباطات رامی تأمین می شود. برخی از ارتباط های رامی ممکن است از دیسک های بین مهره ای عبور کرده و در بافت همبند تعبیه شوند ، که در اعماق منشاء psoas قرار دارد. (Palmgren، Tove، et al.)
دیسک های بین مهره ای دهانه رحم علاوه بر این در جنبه جانبی توسط شاخه های عصب مهره تأمین می شود. اعصاب مهره سینه گردن رحم همچنین مشخص شد که دارای یک مسیر صعودی در کانال مهره هستند که دیسک را در محل ورود آنها و دیگری در بالا تهیه می کنند. (BOGDUK ، NIKOLAI ، و دیگران)
پاتوفیزیولوژی بیماری دژنراسیون دیسک
تقریباً 25٪ از افراد قبل از 40 سالگی تغییرات دژنراتیو دیسک را در بعضی از موارد نشان می دهند. بیش از 40 سال سن ، شواهد MRI در بیش از 60٪ از افراد تغییر می کند. (Suthar، Pokhraj) بنابراین مطالعه فرایند دژنراتیو دیسک های بین مهره ای بسیار مهم است زیرا مشخص شده است که سریعتر از هر بافت همبند دیگری در بدن تخریب می شود و منجر به درد کمر و گردن می شود. تغییرات در سه دیسک بین مهره ای با تغییراتی در بدن و مهره های مهره همراه است که نشانگر یک روند پیشرفتی و پویا است.
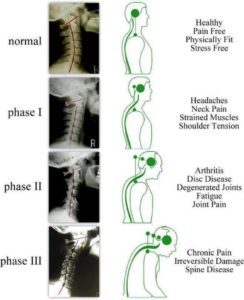
به گفته کرکالدی ویلیس و برنارد ، به نام "آبشار دژنراتیو" ، روند دژنراتیو دیسک های بین مهره ای به سه مرحله تقسیم شده است. این مراحل می توانند با هم همپوشانی داشته باشند و در طول دهه ها رخ دهند. اما شناسایی این مراحل از نظر بالینی به دلیل همپوشانی علائم و نشانه ها امکان پذیر نیست.
مرحله 1 (مرحله تخریب)
این مرحله با تخریب مشخص می شود. تغییرات بافت شناسی وجود دارد ، که اشک و شکاف محیطی را در فیبروز حلقوی نشان می دهد. این اشک های محیطی ممکن است به اشک های شعاعی تبدیل شود و از آنجا که پالپوس آنولوس به خوبی درونی است ، این اشک ها می توانند باعث کمردرد یا درد گردن شوند که موضعی و با حرکات دردناک است. به دلیل ترومای مکرر در دیسک ها ، پلاک ها می توانند جدا شوند که منجر به اختلال در خونرسانی به دیسک و در نتیجه محروم کردن آن از تهیه مواد مغذی و حذف زباله ها می شود. حلقه ممکن است دارای شکستگی های خرد در فیبرهای کلاژن باشد که در میکروسکوپ الکترونی مشاهده می شود و اسکن MRI ممکن است خشکی ، شکاف دیسک و یک ناحیه با شدت زیاد در ناحیه حلقوی را نشان دهد. اتصالات صورت ممکن است یک واکنش سینوویال را نشان دهند و ممکن است باعث درد شدید همراه با سینوویتیت همراه و عدم توانایی در حرکت مفصل در مفاصل زایگاپوفیزیک شود. این تغییرات ممکن است لزوماً در هر فرد رخ ندهد. (گوپتا ، ویجی کومار و دیگران)
هسته پالپوس نیز در این فرآیند دخیل است زیرا ظرفیت جذب آب آن به دلیل تجمع پروتئوگلیکان های تغییر یافته بیوشیمیایی کاهش می یابد. این تغییرات عمدتاً توسط دو آنزیم بنام ماتریس متالوپروتئیناز 3 (MMP-3) و مهار کننده بافت متالوپروتئیناز -1 (TIMP-1) به وجود آمده است. (بهاتنگار ، سوشما و مایناک گپتا) عدم تعادل آنها منجر به از بین رفتن پروتئوگلیکان ها می شود. کاهش ظرفیت جذب آب منجر به کاهش فشار هیدرواستاتیک در هسته پالپوس می شود و باعث می شود تا لام های حلقوی سفت شوند. این می تواند تحرک آن بخش را افزایش داده و منجر به استرس برشی به دیواره حلقوی شود. همه این تغییرات می تواند به فرآیندی به نام لایه لایه شدن حلقوی و شقاق در فیبروز حلقوی منجر شود. این دو فرایند پاتولوژیک جداگانه است و هر دو می توانند منجر به درد ، حساسیت موضعی ، کم تحرکی ، عضلات منقبض شده ، حرکات دردناک مفصل شوند. با این حال ، معاینه عصبی در این مرحله معمولاً طبیعی است.
مرحله 2 (مرحله ناپایداری)
مرحله اختلال عملکرد مرحله ای از بی ثباتی را دنبال می کند که ممکن است ناشی از وخامت تدریجی تمامیت مکانیکی مجموعه مشترک باشد. در این مرحله ممکن است چندین تغییر ایجاد شود ، از جمله اختلال در دیسک و جذب آن ، که می تواند منجر به از بین رفتن ارتفاع فضای دیسک شود. اشک های حلقوی متعدد ممکن است در این مرحله با تغییرات همزمان در مفاصل زاگوفوفیزیال ایجاد شود. اینها ممکن است شامل تخریب غضروف و انعطاف پذیری کپسول صورت باشد که منجر به فرسودگی می شود. این تغییرات بیومکانیکی منجر به ناپایداری بخش تحت تأثیر می شود.
علائمی که در این مرحله دیده می شود مانند مواردی است که در مرحله اختلال عملکرد دیده می شود مانند "دادن راه" از پشت ، درد هنگام ایستادن به مدت طولانی و "گرفتن" در پشت با حرکات. آنها با علائمی مانند حرکات غیرطبیعی مفاصل در هنگام لمس و مشاهده اینکه ستون فقرات پس از ایستادن برای مدتی پس از خم شدن ، به حالت تاب خورده یا به طرف دیگر حرکت می کند ، همراه هستند. (گوپتا ، ویجی کومار و دیگران)
مرحله 3 (مرحله تثبیت مجدد)
در این مرحله سوم و نهایی ، تخریب پیشرونده منجر به باریک شدن فضای دیسک با فیبروز و تشکیل استئوفیت و ایجاد پلهای فرامرزی می شود. درد ناشی از این تغییرات در مقایسه با دو مرحله قبلی شدید است ، اما اینها می تواند بین افراد متفاوت باشد. این باریک شدن فضای دیسک می تواند پیامدهای مختلفی بر ستون فقرات داشته باشد. این می تواند باعث شود کانال کانال بین مهره ای با تقریب پدالهای مجاور در جهت برتر-تحتانی باریک شود. رباط های طولی ، که از ستون مهره ها پشتیبانی می کنند ، ممکن است در بعضی از مناطق که منجر به سستی و بی ثباتی ستون فقرات می شود ، دچار نقص شوند. حرکات ستون فقرات می تواند باعث برآمدگی لیگامنت فلاوم شود و می تواند باعث فرسایش فرایند مفصلی برتر شود. این در نهایت منجر به کاهش قطر در جهت قدامی خلفی فضای بین مهره ای و تنگی کانال های ریشه عصب فوقانی می شود.
تشکیل استئوفیت ها و هیپرتروفی جبه ها می تواند به دلیل تغییر بار محوری بر روی ستون فقرات و مهره ها ایجاد شود. اینها می توانند در هر دو فرآیند مفصلی برتر و تحتانی شکل بگیرند و استئوفیت ها می توانند از کانال بین مهره ای بیرون بیایند در حالی که جنبه هایپرتروفیزه می توانند به سمت کانال مرکزی بیرون زده شوند. تصور می شود که استئوفیت ها از تکثیر غضروف مفصلی در پریوستوم ساخته می شوند و پس از آن تحت عمل کلسیفیکاسیون و استخوانی اندوکندری قرار می گیرند. استئوفیت ها همچنین به دلیل تغییر در تنش اکسیژن و به دلیل تغییر در فشار مایع علاوه بر نقایص توزیع بار تشکیل می شوند. استئوفیت ها و فیبروز پریاتیکولار می توانند منجر به مفاصل سفت شوند. فرآیندهای مفصلی نیز ممکن است در جهت مورب قرار بگیرند و باعث ایجاد رتروپوندیلولیستزیس منجر به باریک شدن کانال بین مهره ای ، کانال ریشه عصبی و کانال نخاعی شود. (KIRKALDY-WILLIS ، WH و دیگران)
همه این تغییرات منجر به کمردرد می شود که با شدت آن کاهش می یابد. علائم دیگری مانند کاهش حرکت ، حساسیت به عضلات ، سفتی و اسکولیوز ایجاد می شود. سلولهای بنیادی سینوویال و ماکروفاژها با آزادسازی فاکتورهای رشد و مولکولهای ماتریکس خارج سلول ، در این فرایند دخیل هستند. مشخص شده است که انتشار سیتوکین ها با هر مرحله همراه است و ممکن است پیامدهای درمانی در توسعه درمان آینده داشته باشد.
اتیولوژی عوامل خطر بیماری دژنراسیون دیسک
پیری و انحطاط
تمایز پیری از تغییرات دژنراتیو دشوار است. پیرس و همكاران اظهار داشته اند كه پیری و دژنراسیون نشان دهنده مراحل پی در پی در طی یك فرآیند واحد است كه در همه افراد اما با نرخ های مختلف اتفاق می افتد. با این حال ، دفع دیسک اغلب با سرعت بیشتری از پیری اتفاق می افتد. بنابراین ، حتی در بیماران در سن کار نیز دیده می شود.
به نظر می رسد بین پیری و انحطاط رابطه وجود دارد ، اما هنوز علت مشخصی مشخص نشده است. مطالعات زیادی در مورد تغذیه ، مرگ سلول و تجمع محصولات ماتریسی تخریب شده و عدم موفقیت هسته انجام شده است. محتوای آب دیسک بین مهره ای با افزایش سن کاهش می یابد. هسته هسته می تواند شکافهایی ایجاد کند که می توانند به داخل فیبروز حلقوی گسترش پیدا کنند. شروع این فرآیند ، chondrosis inter vertebralis نامیده می شود که می تواند نشانه آغاز تخریب دژنراتیو دیسک بین مهره ای ، انتهای صفحه ها و اجسام مهره باشد. این فرآیند باعث ایجاد تغییرات پیچیده در ترکیب مولکولی دیسک می شود و عواقب بیومکانیکی و بالینی دارد که غالباً می تواند منجر به نقص قابل توجهی در فرد مبتلا شود.
غلظت سلول در آنولوس با افزایش سن کاهش می یابد. دلیل اصلی آن این است که سلولهای دیسک تحت پیری قرار می گیرند و توانایی تکثیر را از دست می دهند. سایر دلایل مرتبط با انحطاط مخصوص سن برای دیسک های بین مهره ای شامل از دست دادن سلول ، کاهش تغذیه ، اصلاح پروتئین های ماتریس پس از ترجمه ، تجمع محصولات مولکول های تخریب شده ماتریس و شکست خستگی ماتریس است. کاهش تغذیه به دیسک مرکزی ، که تجمع مواد زائد سلولی و مولکول های تخریب شده ماتریس را امکان پذیر می کند ، مهمترین تغییر در همه این تغییرات به نظر می رسد. این باعث اختلال در تغذیه می شود و باعث کاهش سطح pH می شود ، که می تواند عملکرد سلول را بیشتر به خطر بیندازد و منجر به مرگ سلول شود. افزایش کاتابولیسم و کاهش آنابولیسم سلول های پیر می تواند باعث تحلیل رفتن شود. (باكوالتر ، جوزف آ.) طبق یك مطالعه ، سلولهای پیر در هسته پالپوسوس بیشتر از سلولهای حلقوی فیبروزوس بوده و دیسک های فتق شده شانس بیشتری برای پیری سلول دارند. (Roberts، S. et al.)
هنگامی که روند پیری برای مدتی ادامه می یابد ، غلظت کندرویتین 4 سولفات و کندرویتین 5 سولفات که به شدت آبگریز است ، کاهش می یابد در حالی که نسبت سولفات کراتین به کندرویتین سولفات افزایش می یابد. سولفات کراتان نسبتاً بی آب است و همچنین تمایل کمی به تشکیل سنگدانه های پایدار با اسید هیالورونیک دارد. از آنجا که agrecan تکه تکه شده است ، و وزن و تعداد مولکولی آن کاهش می یابد ، ویسکوزیته و آبگریزی پولیپ هسته را کاهش می دهد. تغییرات دژنراتیو دیسک های بین مهره ای با کاهش فشار هیدرواستاتیک هسته پالپوس و کاهش عرضه مواد مغذی از طریق انتشار تسریع می شود. هنگامی که محتوای آب ماتریکس خارج سلولی کاهش یابد ، ارتفاع دیسک بین مهره ای نیز کاهش می یابد. مقاومت دیسک در برابر بار محوری نیز کاهش می یابد. از آنجا که بار محوری مستقیماً به فیبروز آنولوس منتقل می شود ، شکاف های آنولوس به راحتی پاره می شوند.
همه این مکانیسم ها منجر به تغییرات ساختاری می شوند که در بیماری دیسک دژنراسیون مشاهده می شود. با توجه به کاهش محتوای آب در فیبروز حلقوی و از بین رفتن انطباق ، بار محوری می تواند به جای قسمت قدامی و میانی جنبه های معمولی به جنبه خلفی جبهه ها توزیع شود. این امر می تواند در نتیجه دیسک های دژنراتیو باعث ایجاد آرتروز صورت ، هیپرتروفی در مجاری مهره های مجاور و اسپرز استخوانی یا رشد استخوانی شود که به نام پوکی استخوان معروف است. (چوی ، یونگ سو)
ژنتیک و دژنراسیون
مشخص شده است كه مولفه ژنتيكي يك عامل غالب در بيماري ديسژنرژن ديسك است. مطالعات دوقلوها و مطالعات روی موش ها نشان داده است که ژن ها در تحلیل رفتن دیسک نقش دارند. (بوید ، لارنس ام. ، و دیگران.) ژن هایی که کلاژن I ، IX و XI ، اینترلوکین 1 ، آگرکان ، گیرنده ویتامین D ، متالوپروتئیناز 3 ماتریس (MMP 3) و سایر پروتئین ها را کد می کنند از جمله ژن هایی هستند که پیشنهاد می شود که در بیماری دیسک تحلیل برنده نقش داشته باشد. چندشکلی در آلل های 5 A و 6 A که در ناحیه پروموتر ژن هایی که تولید MMP 3 را تنظیم می کنند اتفاق می افتد ، یک عامل اصلی در افزایش انحطاط دیسک کمر در جمعیت مسن است. فعل و انفعالات در بین این ژن های مختلف به طور کلی به بیماری انحطاط دیسک بین مهره ای کمک می کند.
تغذیه و دژنراسیون
همچنین اعتقاد بر این است که دژنراسیون دیسک به دلیل عدم تأمین مواد مغذی سلولهای دیسک بین مهره ای رخ می دهد. جدای از روند پیری طبیعی ، کمبود تغذیه ای سلولهای دیسکی توسط کلسیفیکاسیون صفحه ، سیگار کشیدن و وضعیت کلی تغذیه تحت تأثیر قرار دارد. کمبود تغذیه می تواند به همراه اسید لاکتیک همراه با فشار کم اکسیژن منجر شود. pH پایین حاصل از آن می تواند بر توانایی سلولهای دیسک در شکل گیری و حفظ ماتریکس خارج سلولی دیسک ها تأثیر بگذارد و باعث تخریب دیسک بین مهره ای شود. دیسک های تخریب شده توانایی پاسخگویی طبیعی به نیروی خارجی را ندارند و حتی ممکن است منجر به اختلالاتی حتی از کوچکترین فشار پشت شوند. (طاهر ، فادی و همکاران)
فاکتورهای رشد سلولهای غضروفی و فیبروبلاستها را تحریک می کنند تا مقدار بیشتری ماتریکس خارج سلولی تولید کنند. همچنین سنتز متالوپروتئینازهای ماتریسی را مهار می کند. نمونه این فاکتورهای رشد شامل تغییر فاکتور رشد ، فاکتور رشد مانند انسولین و فاکتور رشد اساسی فیبروبلاست است. ماتریس تخریب شده با افزایش سطح رشد فاکتور رشد و فاکتور رشد فیبروبلاست اساسی ترمیم می شود.
محیط زیست و دژنراسیون
حتی اگر همه دیسک ها از یک سن باشند ، دیسک های یافت شده در قسمت های کمر پایین نسبت به دیسک های موجود در قسمت فوقانی در برابر تغییرات دژنراتیو آسیب پذیرتر هستند. این نشان می دهد که نه تنها پیری بلکه بارگذاری مکانیکی نیز یک عامل ایجاد کننده است. ارتباط بین بیماری دیسک تحلیل برنده و عوامل محیطی به صورت جامع توسط ویلیامز و سامبروک در سال 2011 تعریف شده است. (ویلیامز ، FMK و PN سامبروک) بار فیزیکی سنگین مرتبط با شغل شما یک عامل خطر است که تا حدی به دیسک کمک می کند. بیماری دژنراتیو بر اساس برخی مطالعات ، احتمال وجود مواد شیمیایی باعث تحلیل رفتن دیسک مانند سیگار کشیدن نیز وجود دارد. (Batti ، Michele C.) نیکوتین در تحقیقات دوقلویی نقش دارد که باعث اختلال در جریان خون در دیسک بین مهره ای می شود و منجر به تحلیل رفتن دیسک می شود. (BATTI ، MICHELE C. ، et al.) علاوه بر این ، ارتباطی در بین ضایعات آترواسکلروتیک در آئورت و کمردرد به دلیل ارتباط بین تصلب شرایین و بیماری دژنراتیو دیسک یافت شده است. (Kauppila، LI) شدت تخریب دیسک در اضافه وزن ، چاقی ، سندرم متابولیک و افزایش شاخص توده بدن نقش دارد. ("یک مطالعه مبتنی بر جمعیت" از انحطاط دیسک نوجوانان و ارتباط آن با اضافه وزن و چاقی ، کمردرد و وضعیت عملکردی کاهش یافته. Samartzis D، Karppinen J، Mok F، Fong DY، Luk KD، Cheung KM. J Bone Joint Surg صبح 2011 ؛ 93 (7): 662 70 )
درد در دژنراسیون دیسک (درد دیسکوژنیک)
درد دیسکوژنیک ، که نوعی درد دردی است ، هنگامی که سیستم عصبی تحت تأثیر بیماری تحلیل برنده دیسک قرار می گیرد ، از مفصل دهنده های حلقوی فیبروزوس ناشی می شود. Annulus fibrosus حاوی فیبرهای عصبی واکنشی ایمنی در لایه خارجی دیسک با سایر مواد شیمیایی مانند پلی پپتید روده ای واسواکتیو ، پپتید مربوط به ژن کلسی تونین و ماده P. (KONTTINEN ، YRJ T. و همکاران) است دیسک های بین مهره ای رخ می دهد ، ساختار طبیعی و بار مکانیکی تغییر می کند که منجر به حرکات غیر طبیعی می شود. این مفصل گیرنده های دیسک می توانند به طور غیر طبیعی به محرک های مکانیکی حساس شوند. این درد همچنین می تواند در اثر pH کم ناشی از وجود اسید لاکتیک ایجاد شود و باعث افزایش تولید واسطه های درد شود.
درد ناشی از بیماری دیسک دژنراتیو ممکن است از ریشه های متعدد ناشی شود. ممکن است به دلیل آسیب ساختاری ، فشار و تحریک روی اعصاب ستون فقرات ایجاد شود. دیسک به خودی خود فقط حاوی چند فیبر عصبی است ، اما هرگونه صدماتی می تواند این اعصاب یا همان رباط های طولی خلفی را حساس کند و باعث ایجاد درد شود. میکرو حرکات در مهره ها ممکن است اتفاق بیفتد که ممکن است باعث اسپاسم عضلانی رفلکس دردناک شود زیرا دیسک آسیب دیده و فرسوده با از بین رفتن تنش و ارتفاع ایجاد می شود. حرکات دردناک بوجود می آید زیرا اعصاب تأمین کننده ناحیه توسط مفاصل و لیگامانهای صورت در لبه فشرده یا تحریک می شوند که منجر به درد پا و کمر می شود. این درد ممکن است با آزاد شدن پروتئینهای التهابی که بر روی اعصاب موجود در فورامن یا اعصاب نزولی در کانال ستون فقرات عمل می کنند ، تشدید شود.
نمونه های پاتولوژیک دیسک های دژنراتیو ، هنگامی که در زیر میکروسکوپ مشاهده می شوند ، نشان می دهد که بافت های گرانول عروقی و حرکات گسترده ای وجود دارد که در شکاف های لایه بیرونی فیبروز آنولوس گسترش یافته به پولیپوس هسته وجود دارد. ناحيه بافت گرانول توسط سلول هاي ماستيك فراواني نفوذ مي كند و آنها به طور هم زمان در فرآيند هاي آسيب شناسي نقش دارند كه در نهايت منجر به درد ناشي مي شوند. این موارد شامل نئوواسکولاریزاسیون ، دژنراسیون دیسک بین مهره ای ، التهاب بافت دیسک و تشکیل فیبروز است. سلول های ماست همچنین موادی مانند فاکتور نکروز تومور و اینترلوکین ها را آزاد می کنند که ممکن است برای فعال شدن برخی مسیرهایی که در ایجاد کمردرد نقش دارند ، نشانه گذاری کنند. مواد دیگری که می توانند این مسیرها را تحریک کنند عبارتند از فسفولیپاز A2 ، که از آبشار اسید آراشیدونیک تولید می شود. این ماده در افزایش غلظت در قسمت سوم بیرونی دیسک دژنراتیو یافت می شود و تصور می شود که باعث تحریک درد گیرنده های مستقر در آنجا برای انتشار مواد التهابی برای ایجاد درد می شود. این مواد باعث آسیب آکسون ، ادم داخلی و دمیلینه شدن می شوند. (بریزبی ، هلنا)
تصور می شود که کمر درد از خود دیسک بین مهره ای ناشی می شود. از این رو با گذشت زمان و قطع دیسک تحلیل برنده ، درد به تدریج کاهش می یابد. با این حال ، درد در واقع بر اساس مطالعات آندوسکوپی فقط در 11٪ از بیماران از خود دیسک ناشی می شود. به نظر می رسد علت واقعی کمردرد به دلیل تحریک مرز داخلی عصب است و به نظر می رسد درد ارجاعی در امتداد بازو یا پا به دلیل تحریک هسته عصب ایجاد می شود. درمان دژنراسیون دیسک عمدتا باید بر کاهش درد جهت کاهش درد و رنج بیمار متمرکز باشد زیرا این ناتوان کننده ترین علامتی است که زندگی بیمار را مختل می کند. بنابراین ، ایجاد مکانیسم درد مهم است زیرا این امر نه تنها به دلیل تغییرات ساختاری در دیسک های بین مهره ای اتفاق می افتد ، بلکه همچنین به دلیل عوامل دیگر مانند انتشار مواد شیمیایی و درک این مکانیسم ها می تواند منجر به تسکین م effectiveثر درد شود. (چوی ، یونگ سو)
ارائه بالینی بیماری دیسک انحطاطی
بیماران مبتلا به بیماری دیسک دژنراتیو بسته به محل بیماری با تعداد بیشماری از علائم روبرو هستند. كسانی كه دچار دژنراسیون دیسک کمر هستند ، کمردرد ، علائم رادیکول و ضعف دارند. کسانی که دچار دژنراسیون دیسک گردنی هستند ، درد گردن و شانه دارند.
کمردرد می تواند با حرکات و موقعیت تشدید شود. معمولاً علائم با انعطاف بدتر می شوند ، در حالی که پسوند اغلب آنها را تسکین می دهد. جراحات پیچشی جزئی ، حتی ناشی از تاب خوردن یک گلف ، می تواند علائم را تحریک کند. معمولاً درد هنگام راه رفتن یا دویدن ، هنگام تغییر وضعیت به طور مکرر و دراز کشیدن کمتر است. با این حال ، این درد معمولاً ذهنی است و در بسیاری از موارد ، از فردی به فرد دیگر به میزان قابل توجهی متفاوت است و بیشتر افراد به طور مداوم از یک سطح کم درد مزمن در ناحیه کمر رنج می برند ، در حالی که گاهی اوقات از کشاله ران ، ران و ساق پا رنج می برند. شدت درد هر از گاهی افزایش می یابد و چند روز ادامه خواهد داشت و به تدریج فروکش می کند. این "شعله ور شدن" یک دوره حاد است و باید با مسکن های قوی درمان شود. درد بدتر در حالت نشسته احساس می شود و در حین خم شدن ، بلند کردن و چرخاندن مرتب حرکات تشدید می شود. شدت درد می تواند به میزان قابل توجهی متفاوت باشد ، در بعضی از آنها گاهی اوقات درد خسته کننده ای ایجاد می شود و در برخی دیگر به طور متناوب درد شدید و ناتوان کننده وجود دارد. (جیسون م. هایسمیت ، MD)
درد و حساسیت موضعی در ستون فقرات محوری معمولاً ناشی از درد گیرنده های موجود در دیسک های بین مهره ای ، مفاصل صورت ، مفاصل ساکروایلیاک ، دورا مایع ریشه های عصبی و ساختارهای میوفاشیال موجود در ستون فقرات محوری است. همانطور که در بخش های قبلی ذکر شد ، تغییرات آناتومیکی انحطاطی ممکن است منجر به تنگ شدن کانال نخاعی به نام تنگی نخاع ، رشد بیش از حد فرآیندهای نخاعی به نام استئوفیس ها ، هیپرتروفی فرآیندهای مفصلی تحتانی و برتر ، اسپوندیلولیستزی ، گل شدن لیگامنت فلاوم و فتق دیسک شود. . این تغییرات منجر به مجموعه ای از علائم می شود که به عنوان تبانی عصبی شناخته می شود. ممکن است علائمی مانند کمردرد و درد پا همراه با بی حسی یا سوزن شدن در پاها ، ضعف عضلات و افتادگی پا وجود داشته باشد. از بین رفتن کنترل روده یا مثانه ممکن است نشان دهنده ضعف نخاع باشد و برای جلوگیری از ناتوانی دائمی نیاز به مراقبت پزشکی سریع است. این علائم می توانند از نظر شدت متفاوت باشند و ممکن است در افراد مختلف به میزان های مختلفی بروز کند.
این درد همچنین می تواند به سایر نقاط بدن تابیده شود به دلیل اینكه نخاع به دو محل مختلف بدن چندین شاخه می دهد. بنابراین ، هنگامی که دیسک تخریب شده بر روی ریشه عصب نخاعی فشار می آورد ، درد را می توان در پا نیز تجربه کرد که عصب در نهایت در آن غرق می شود. این پدیده با نام رادیکولوپاتی به دلیل فرایند دژنراسیون می تواند از بسیاری از منابع ناشی از آن بوجود آید. دیسک شکاف ، اگر به صورت مرکزی بیرون زده باشد ، می تواند بر نزول ریشه های شبکیه شبکیه تأثیر بگذارد ، اگر بصورت خلفی به صورت برآمدگی ایجاد شود ، ممکن است روی ریشه های عصبی خارج شده در کانال تحتانی تحتانی بعدی تأثیر بگذارد و عصب ستون فقرات در داخل راموس شکمی آن هنگام بیرون زدگی دیسک تأثیر بگذارد. جانبی به طور مشابه ، استئوفیت های بیرون زده در حاشیه های فوقانی و تحتانی از جنبه خلفی بدن مهره ها می توانند بر روی همان بافت های عصبی ضربه بزنند و همین علائم را ایجاد می کنند. هیپرتروفی فرآیند مفصلی نیز بسته به نوع بینی آنها ممکن است بر ریشه های عصبی آسیب برساند. عصب ها ممکن است قبل از خارج شدن از کانال تحتانی بعدی کانال بین مهره ای و ریشه های عصبی در کانال ریشه عصب فوقانی و کیسه دهانه شامل ریشه های عصبی باشد. این علائم ، به دلیل اختلال در اعصاب ، توسط مطالعات cadaver اثبات شده است. تصور می شود مصالحه عصبی هنگامی اتفاق بیفتد که قطر لایه سازه عصبی با کاهش 70 درصدی مسدود شود. علاوه بر این ، سازگاری عصبی می تواند هنگامی ایجاد شود که دیسک خلفی کمتر از 4 میلی متر از ارتفاع فشرده شود ، یا وقتی که ارتفاع foraminal به کمتر از 15 میلی متر کاهش می یابد و منجر به تنگی فرمامینال و ضربات عصبی می شود. (طاهر ، فادی و همکاران)
رویکرد تشخیصی
در ابتدا بیماران با سابقه دقیق و معاینه کامل جسمی و تحقیقات مناسب و آزمایشات تحریک آمیز ارزیابی می شوند. با این حال ، تاریخ به دلیل درد مزمن که نمی تواند بطور صحیح بومی سازی شود و مشکل در تعیین محل دقیق آناتومیک در حین آزمایش تحریک آمیز به دلیل تأثیر ساختارهای آناتومیکی همسایه ، اغلب مبهم است.
از طریق تاریخچه بیمار ، می توان علت کمردرد را ناشی از مفصل درد در دیسک های بین مهره ای تشخیص داد. بیماران همچنین ممکن است سابقه ماهیت مزمن علائم و بی حسی مربوط به ناحیه گلوتئال ، سوزن سوزن شدن و همچنین سفتی در ستون فقرات را نشان دهند که معمولاً با فعالیت بدتر می شود. حساسیت ممکن است با لمس روی ستون فقرات ایجاد شود. به دلیل ماهیت و دردناک بودن بیماری ، بیشتر بیماران ممکن است از اختلالات خلقی و اضطرابی رنج ببرند. تصور می شود که افسردگی به طور منفی در بار بیماری نقش دارد. با این حال ، هیچ ارتباط واضحی بین شدت بیماری و اختلالات خلقی یا اضطرابی وجود ندارد. خوب است که در مورد این شرایط بهداشت روان نیز هوشیار باشیم. به منظور حذف سایر آسیب های جدی ، باید س questionsالاتی در مورد خستگی ، کاهش وزن ، تب و لرز مطرح شود ، که ممکن است برخی بیماری های دیگر را نشان دهد. (جیسون ام. هایزمیت ، MD)
علت دیگری که برای کمردرد وجود دارد باید هنگام معاینه بیمار از بیماری دیسک دژنراتیو جدا شود. آسیب شناسی شکم ، که می تواند باعث کمردرد مانند آنوریسم آئورت ، کلیه های کلیوی و بیماری لوزالمعده شود ، باید از این امر مستثنا شوند.
بیماری دژنراتیو دیسک چندین تشخیص افتراقی دارد که باید در هنگام مراجعه بیمار به کمردرد مورد بررسی قرار گیرد. این شامل؛ کمردرد ایدیوپاتیک ، تخریب مفصل زیگاپوفیزی ، میلوپاتی ، تنگی کمر ، اسپوندیلوز ، آرتروز و رادیکولوپاتی کمر. (Disc بیماری دیسک دژنراتیو فیزیوپدیا )
تحقیقات
تحقیقات برای تأیید تشخیص بیماری دیسک دژنراسیون استفاده می شود. اینها را می توان به مطالعات آزمایشگاهی ، مطالعات تصویربرداری ، آزمایش هدایت عصب و روشهای تشخیصی تقسیم کرد.
مطالعات تصویربرداری
تصویربرداری در بیماری دیسک انحطاطی عمدتا برای توصیف روابط آناتومیکی و ویژگیهای مورفولوژیکی دیسک های آسیب دیده استفاده می شود ، که دارای ارزش درمانی زیادی در تصمیم گیری های آینده برای گزینه های درمانی است. هر روش تصویربرداری ، مانند رادیوگرافی ساده ، CT یا MRI ، می تواند اطلاعات مفیدی را ارائه دهد. با این حال ، تنها در 15٪ بیماران می توان علت اصلی را یافت زیرا در صورت عدم وجود فتق دیسک و نقص عصبی ، هیچ تغییر رادیولوژیکی واضحی در بیماری دیسک تخریب دیده نمی شود. علاوه بر این ، هیچ ارتباطی بین تغییرات آناتومیکی مشاهده شده در تصویربرداری و شدت علائم وجود ندارد ، اگرچه بین تعداد استئوفیت ها و شدت کمر همبستگی وجود دارد. تغییرات دژنراتیو در رادیوگرافی همچنین در افراد بدون علامت دیده می شود که منجر به مشکل در انطباق ارتباط بالینی و زمان شروع درمان می شود. (Disc بیماری دیسک دژنراتیو فیزیوپدیا )
رادیوگرافی ساده
این رادیوگرافی ساده و در دسترس راديوگرافی ساده گردن رحم می تواند اطلاعات مهمی در مورد ناهنجاری ها ، تراز شدن و تغییرات استخوانی دژنراتیو ارائه دهد. به منظور تعیین وجود ناپایداری ستون فقرات و تعادل ساژیتال ، خم شدن پویا یا مطالعات اکستنشن باید انجام شود.
تصویربرداری رزونانس مغناطیسی (MRI)
MRI متداول ترین روش برای تشخیص تغییرات تحلیل برنده در دیسک بین مهره ای به طور دقیق ، مطمئن و جامع است. در ارزیابی اولیه بیماران مبتلا به گردن درد پس از رادیوگرافی ساده استفاده می شود. این می تواند تصاویر غیرتهاجمی را در چندین دشت فراهم کند و تصاویر با کیفیت عالی از دیسک را ارائه می دهد. MRI می تواند هیدراتاسیون دیسک و مورفولوژی را براساس چگالی پروتون ، محیط شیمیایی و محتوای آب نشان دهد. هنگام تفسیر گزارشهای MRI باید تصویر بالینی و سابقه بیمار در نظر گرفته شود زیرا نشان داده شده است که در صورت وجود اطلاعات بالینی ، 25٪ از رادیولوژیستها گزارش خود را تغییر می دهند. Fonar اولین اسکنر MRI باز را با توانایی بیمار برای اسکن در موقعیت های مختلف مانند ایستادن ، نشستن و خم شدن تولید کرد. به دلیل این ویژگی های منحصر به فرد ، این اسکنر MRI باز می تواند برای اسکن بیماران در حالت های تحمل کننده وزن و ایستادن به حالت ایستاده برای شناسایی تغییرات زمینه ای پاتولوژیک باشد که معمولاً در اسکن MRI معمولی مانند بیماری دیسک تحلیل برنده کمر با فتق نادیده گرفته می شود. این دستگاه برای بیماران کلاستروفوبیک نیز مناسب است ، زیرا آنها در طول اسکن به تماشای یک صفحه تلویزیون بزرگ می روند. (e بیماری دیسک دژنراتیو: زمینه ، آناتومی ، پاتوفیزیولوژی. )
Nucleus pulposus و فیبروز حلقوی دیسک معمولاً در MRI قابل شناسایی است و منجر به تشخیص فتق دیسک به صورت موجود و غیر موجود می شود. از آنجا که MRI همچنین می تواند اشک های حلقوی و رباط طولی خلفی را نشان دهد ، می توان از آن برای طبقه بندی فتق استفاده کرد. این می تواند یک حلقه حلقوی ساده به فتق دیسک قطعه ای آزاد باشد. این اطلاعات می تواند دیسک های آسیب شناسی مانند دیسک اکسترود شده ، دیسک های بیرون زده و دیسک های مهاجرت را توصیف کند.
چندین سیستم درجه بندی بر اساس شدت سیگنال MRI ، ارتفاع دیسک ، تمایز بین هسته و حلقه و ساختار دیسک وجود دارد. این روش ، توسط Pfirrmann و همکاران ، به طور گسترده ای مورد استفاده قرار گرفته و از نظر بالینی پذیرفته شده است. طبق سیستم اصلاح شده ، 8 درجه برای بیماری دژنراسیون دیسک کمر وجود دارد. درجه 1 دیسک بین مهره ای طبیعی را نشان می دهد و درجه 8 مطابق با مرحله آخر انحطاط است ، پیشرفت بیماری دیسک را نشان می دهد. تصاویر مربوطه برای کمک به تشخیص وجود دارد. از آنجا که تمایز بافت خوبی دارند و شرح مفصلی از ساختار دیسک را ارائه می دهند ، از تصاویر دارای وزنی Tagittal T2 برای طبقه بندی استفاده می شود. (پفییرمن ، مسیحی WA ، و دیگران)
موديك تغييرات رخ داده در بدن مهره هاي مجاور ديسك هاي دژنراسيون را به عنوان تغييرات نوع 1 و نوع 2 توصيف كرده است. در تغییرات Modic 1 ، شدت تصاویر با وزن T1 و تصاویر با شدت T2 با شدت کاهش می یابد. تصور می شود این اتفاق می افتد زیرا صفحات انتهایی تحت اسکلروز قرار گرفته و مغز استخوان مجاور با افزایش ضریب انتشار ، پاسخ التهابی را نشان می دهد. این افزایش ضریب انتشار و مقاومت نهایی در برابر انتشار توسط مواد شیمیایی آزاد شده از طریق مکانیسم خود ایمنی حاصل می شود. تغییرات نوع 2 شامل تخریب مغز استخوان پلاک های مهره ای مجاور به دلیل پاسخ التهابی و نفوذ چربی در مغز است. این تغییرات ممکن است منجر به افزایش تراکم سیگنال در تصاویر دارای وزن T1 شود. (Modic، MT و همکاران)
توموگرافی کامپیوتری (CT)
هنگامی که MRI در دسترس نباشد ، توموگرافی کامپیوتری یک آزمایش تشخیصی در نظر گرفته می شود که می تواند فتق دیسک را تشخیص دهد ، زیرا تضاد بهتری بین حاشیه های خلفی طرف مقابل مهره های استخوانی مجاور ، چربی پرینه و مواد فتق دیسک دارد. با این وجود ، هنگام تشخیص فتق های جانبی ، MRI حالت انتخاب تصویربرداری باقی مانده است.
سی تی اسکن دارای چندین مزیت نسبت به MRI است ، از جمله اینکه دارای یک محیط کلاستروفوبیک کمتری ، هزینه کم و تشخیص بهتر تغییراتی است که ظریف است و ممکن است در سایر روشها نیز از دست برود. CT می تواند تغییرات دژنراتیو اولیه مفاصل صورت و اسپوندیلوز را با دقت بیشتر تشخیص دهد. یکپارچگی استخوان پس از همجوشی نیز با استفاده از CT بهترین ارزیابی است.
با استفاده از معیارهای ایجاد شده توسط گوندری و هایتوف ، فتق دیسک و عصب همراه است. برای بیرون زدگی دیسک بسیار مهم است که مستقیماً روی ریشه های عصبی که در حال گذر از دیسک می باشند دراز بکشند و دارای موقعیت کانونی و نامتقارن باشند. فشرده سازی یا جابجایی ریشه عصبی قابل اثبات است. سرانجام ، دیستال اعصاب در اثر انقباض (محل فتق) اغلب با ورم ناشی از برجستگی ، برجستگی رگهای اپیدورال مجاور و اگزوداتهای التهابی منجر به بزرگ شدن و برآمدگی می شود.
کمری Dایزوگرافی
این روش بحث برانگیز است و اینکه دانستن محل درد درمورد جراحی هیچ ارزشی دارد یا خیر ، اثبات نشده است. مثبت کاذب می تواند به دلیل هیپرآلژزی مرکزی در بیماران مبتلا به درد مزمن (یافته عصبی و فیزیولوژیکی) و به دلیل عوامل روانی- اجتماعی رخ دهد. درست است که درد دژنوژن از نظر بالینی قابل توجه باشد ، جای سوال دارد. کسانی که از این تحقیق حمایت می کنند ، از معیارهای دقیق برای انتخاب بیماران و در هنگام تفسیر نتایج حمایت می کنند و معتقدند این تنها آزمایش است که می تواند درد دلسوز را تشخیص دهد. دیسکوگرافی کمری را می توان در چندین موقعیت استفاده کرد ، اگرچه از نظر علمی تثبیت نشده است. این شامل؛ تشخیص فتق جانبی ، تشخیص دیسک علامت دار در بین ناهنجاری های متعدد ، ارزیابی ناهنجاری های مشابه دیده شده در CT یا MRI ، ارزیابی ستون فقرات بعد از عمل ، انتخاب سطح فیوژن و ویژگی های مطرح کننده وجود درد discogenic.
دیسکوگرافی بیشتر از تعیین آناتومی دیسک نگران ایجاد پاتوفیزیولوژی است. بنابراین ، ارزیابی درد discogenic هدف از دیسکوگرافی است. MRI ممکن است یک دیسک غیر طبیعی و بدون درد را نشان دهد ، در حالی که درد شدید ممکن است در دیسکوگرافی مشاهده شود که یافته های MRI تعداد کمی دارند. در هنگام تزریق نمک نرمال یا مواد کنتراست ، یک نقطه انتهایی اسفنجی با دیسک های غیر طبیعی می تواند مقادیر بیشتری از کنتراست را بپذیرد. ماده کنتراست می تواند از طریق اشک و شکاف در فیبروز حلقوی در دیسک های غیر طبیعی به پالپوس هسته برسد. فشار این ماده حاجب می تواند به دلیل درونی شدن عصب منیژنی مکرر ، عصب ترکیبی نخاع ، رامی اولیه قدامی و رامی کمونیست خاکستری که فیبروز آنولوس بیرونی را تأمین می کند ، درد را تحریک کند. هنگامی که ماده حاجب به محل آسیب ریشه عصبی توسط دیسک غیرطبیعی برسد ، درد رادیکولار تحریک می شود. با این حال ، این آزمایش دیسکوگرافی دارای عوارض مختلفی از جمله آسیب ریشه عصبی ، دیسکیت شیمیایی یا باکتریایی ، حساسیت به کنتراست و تشدید درد است. (بارتینسکی ، والتر س. ، و ا. اورلاندو اورتیز)
تصویربرداری ترکیب
به منظور ارزیابی فشرده سازی ریشه عصب و تنگی دهانه رحم به درستی ، ممکن است ترکیبی از روش های تصویربرداری مورد نیاز باشد.
سی تی اسکن
پس از انجام دیسکوگرافی اولیه ، دیسکوگرافی CT در طی 4 ساعت انجام می شود. می توان از آن برای تعیین وضعیت دیسک مانند فتق ، بیرون زده ، اکسترود ، حاوی یا توقیف استفاده کرد. همچنین می تواند در ستون فقرات مورد استفاده قرار گیرد تا اثرات جمعی بافت اسکار یا مواد دیسک را بعد از عمل جراحی ستون فقرات تمایز دهد.
میلوگرافی CT
این آزمایش بهترین روش برای ارزیابی فشرده سازی ریشه عصبی در نظر گرفته می شود. هنگامی که سی تی اسکن به صورت ترکیبی یا بعد از میلوگرافی انجام می شود ، می توان جزئیات مربوط به آناتومی استخوانی هواپیماهای مختلف را با سهولت نسبی بدست آورد.
روشهای تشخیصی
بلوک های ریشه عصبی انتخابی ترانسفرمینال (SNRBs)
هنگامی که بیماری دیسک تخریب کننده چند سطحی در اسکن MRI مشکوک است ، از این آزمایش می توان برای تعیین ریشه عصبی خاص که تحت تأثیر قرار گرفته استفاده شود. SNRB هم تست تشخیصی و هم درمانی است که می تواند برای تنگی نخاع کمر مورد استفاده قرار گیرد. این آزمایش با تزریق ماده بی حسی و ماده حاجب تحت هدایت فلوروسکوپی به سطح ریشه عصبی علاقه مند ، ناحیه ای از میزان افت فشار خون را ایجاد می کند. بین علائم بالینی بیماری دژنراتیو دیسک گردنی چند وجهی و یافته های MRI و یافته های SNRB مطابق با اندربرگ و همبستگی وجود دارد. ارتباط 28٪ با نتایج SNRB و درد رادیکولی پوستی و مناطق با نقص عصبی وجود دارد. بیشترین موارد تخریب در MRI با 60 درصد ارتباط دارد. اگرچه بطور معمول مورد استفاده قرار نمی گیرد ، SNRB یک آزمایش مفید برای ارزیابی بیماران قبل از عمل در بیماری دیسک دژنراتیو چند سطحی به خصوص در ستون فقرات به همراه ویژگی های بالینی و یافته های MRI است. (نارویز ، سامر و امارشه ویدیاناتان)
مطالعات الکترو میوگرافی
آزمایشات هدایت عصب حرکتی و حسی دیستال ، تحت عنوان مطالعات الکترومیوگرافی ، که با معاینه سوزن غیرطبیعی طبیعی هستند ، ممکن است علائم فشرده سازی عصب را که در تاریخچه بالینی ایجاد می شود ، نشان دهد. ریشه های عصبی تحریک پذیر را می توان با استفاده از تزریق برای بی حسی اعصاب آسیب دیده یا گیرنده های درد در فضای دیسک ، مفصل ساکروایلیاک یا مفاصل وجهی توسط دیسکوگرافی. ("ژورنال تقویم الکترومیوگرافی و حرکت شناسی")
مطالعات آزمایشگاهی
آزمایشات آزمایشگاهی معمولاً انجام می شود تا سایر تشخیص های افتراقی از بین برود.
از آنجایی که اسپوندیلوآرتروپاتی های سروتونگاتیو ، مانند اسپوندیلیت آنکیلوزان ، دلایل عمده کمردرد هستند ، بایستی سازگاری سیستم ایمنی HLA B27 را آزمایش کند. تخمین زده می شود 350,000 نفر در ایالات متحده و 600,000 نفر در اروپا تحت تأثیر این بیماری التهابی ناشی از علت ناشناخته قرار گرفته اند. اما HLA B27 به ندرت در آمریکایی های آفریقایی یافت می شود. سایر اسپوندیلوآرتروپاتی های سروتونگاتیو که می توانند با استفاده از این ژن آزمایش شوند شامل آرتریت پسوریاتیک ، بیماری التهابی روده و آرتریت واکنشی یا سندرم رایتیر است. ایمونوگلوبولین A سرم (IgA) در برخی بیماران افزایش می یابد.
تست هایی مانند میزان رسوب گلبول های قرمز (ESR) و تست سطح پروتئین واکنشی C (CRP) برای واکنش دهنده های فاز حاد که در علل التهابی کمردرد مانند استئوآرتریت و بدخیمی مشاهده می شود. شمارش کامل خون نیز برای تعیین علت بیماری لازم است ، از جمله شمارش های دیفرانسیل. بیماریهای خود ایمنی هنگام مثبت شدن فاکتور روماتوئید (RF) و آنتی بادی ضد هسته ای (ANA) مشکوک می شوند. تجزیه اسید اوریک و مایع سینوویال سرم در مورد کریستالها ممکن است در موارد نادری برای حذف رسوب دیهیدرات نقره و پیروفسفات مورد نیاز باشد.
رفتار
هیچ روش درمانی قطعی در مورد معالجه بیماری دیسک دژنراتیو توسط کلیه پزشکان وجود ندارد زیرا علت درد در افراد مختلف می تواند متفاوت باشد و همچنین شدت درد و تغییرات گسترده در ارائه بالینی وجود دارد. در مورد گزینه های درمانی می توان به طور گسترده ای مورد بحث قرار گرفت. درمان محافظه کارانه ، معالجه پزشکی و معالجه جراحی.
درمان محافظه کار
این روش درمانی شامل تمرین درمانی با مداخلات رفتاری ، روشهای جسمی ، تزریقات ، آموزش پشت و روشهای برگشت به مدرسه است.
درمان مبتنی بر ورزش با مداخلات رفتاری
بسته به تشخیص بیمار ، انواع مختلفی از تمرینات قابل تجویز است. این یکی از اصلی ترین روش های مدیریت محافظه کارانه برای درمان کمردرد مزمن است. تمرینات را می توان اصلاح کرد که شامل تمرین های کششی ، تمرین های هوازی و تمرین های تقویت عضله است. یکی از مهمترین چالش های این روش درمانی ، عدم توانایی آن در ارزیابی اثربخشی در بیماران به دلیل تغییرات گسترده در رژیم های ورزشی ، فراوانی و شدت آن است. طبق مطالعات ، بیشترین اثربخشی در کمردرد حاد با مدت زمان مختلف علائم با انجام برنامه های تمرینی درجه بندی شده در محیط شغلی بیمار به دست آمده است. با توجه به بهبود عملکرد و کاهش درد ، در بین بیمارانی که از علائم مزمن رنج می برند ، پیشرفت های چشمگیری مشاهده شد. به نظر می رسد روشهای درمانی اختصاصی که برای هر بیمار تحت نظارت و رعایت دقیق بیمار طراحی شده است ، در افراد مبتلا به کمردرد مزمن مؤثرترین است. از دیگر رویکردهای محافظه کارانه برای بهبود این رویکرد می توان در ترکیب استفاده کرد. (هایدن ، جیل ا. ، و دیگران)
تمرینات هوازی اگر به طور مرتب انجام شود ، می تواند استقامت را بهبود بخشد. برای تسکین تنش ماهیچه ها می توان از روش های آرام سازی استفاده کرد شنا همچنین یک تمرین برای کمردرد محسوب می شود. تمرینات کف می تواند شامل تمرینات کششی ، کشش همسترینگ ، حرکات کششی کمر ، کشش مچ دست تا زیر چانه ، آسانسور صندلی ، نشستن اصلاح شده ، برآمدگی شکم و تمرین های کوهستانی و ساحلی باشد.
روشهای جسمی
این روش شامل استفاده از تحریک عصب الکتریکی ، آرامش ، بستههای یخی ، بیوفیدبک ، پدهای گرمایش ، فونوفورز و یوناتوفورز است.
تحریک عصب الکتریکی از راه پوست (TENS)
در این روش غیر تهاجمی ، تحریک الکتریکی به منظور تحریک اعصاب محیطی در منطقه برای تحریک درد تا حدودی تحریک شده و به پوست تحویل داده می شود. این روش بلافاصله پس از استفاده از درد تسکین می یابد ، اما اثر طولانی مدت آن مشکوک است. با برخی از مطالعات ، مشخص شده است که در مقایسه با دارونما بهبود معنی داری در درد و وضعیت عملکردی وجود ندارد. دستگاه های انجام این TENS را می توان از بخش سرپایی به راحتی در دسترس قرار داد. به نظر می رسد تنها عارضه جانبی آن یک تحریک خفیف پوست است که در یک سوم بیماران تجربه می شود. (جانسون ، مارك اول)
مدرسه برگشت
این روش با هدف کاهش علائم درد و عودهای آنها معرفی شده است. این نخستین بار در سوئد معرفی شد و وضعیت بدن ، ارگونومی ، تمرینات مناسب پشت و آناتومی ناحیه کمر را در نظر می گرفت. به بیمار نحوه صحیح نشستن ، ایستادن ، بلند کردن وزنه ها ، خوابیدن ، شستن صورت و مسواک زدن از دندان ها یاد داده می شود. در مقایسه با سایر روشهای درمانی ، ثابت شده است که درمان در مدرسه برگشت در هر دو دوره فوری و متوسط برای بهبود درد کمر و وضعیت عملکردی مؤثر است.
آموزش بیمار
در این روش ، ارائه دهنده به بیمار می آموزد که چگونه علائم کمردرد خود را مدیریت کند. ابتدا آناتومی و ستون فقرات نرمال ستون فقرات و بیومکانیک شامل مکانیسم های آسیب دیدگی آموزش داده می شود. در مرحله بعد ، با استفاده از مدل های ستون فقرات ، تشخیص بیماری دژنراتیو دیسک برای بیمار توضیح داده می شود. برای فرد بیمار ، موقعیت متعادل تعیین می شود و از آن خواسته می شود تا برای جلوگیری از بروز علائم ، آن موقعیت را حفظ کند.
رویکرد زیست روانشناختی به درمان با چند رشته ای
کمردرد می تواند ناراحتی زیادی را برای بیمار ایجاد کند و منجر به اختلالات روانشناختی و روحیه پایین شود. این می تواند بر نتایج درمانی تأثیر منفی بگذارد و باعث بیهوده ترین استراتژی های درمانی شود. بنابراین ، بیماران باید در مورد استراتژی های شناختی یاد گرفته شده به نام "رفتاری" و "استراتژی های روانی-اجتماعی" آموزش ببینند تا از درد راحت شوند. علاوه بر درمان علل بیولوژیکی درد ، باید علل روانشناختی و اجتماعی نیز در این روش مورد توجه قرار گیرد. به منظور کاهش درک بیمار از درد و ناتوانی ، از روشهایی مانند انتظارات اصلاح شده ، روشهای آرام سازی ، کنترل پاسخهای فیزیولوژیکی با رفتار آموخته شده و تقویت استفاده می شود.
ماساژ درمانی
برای کمردرد مزمن ، به نظر می رسد این روش درمانی مفید است. در طی یک دوره 1 ساله ، مشخص شده است که ماساژ درمانی در مقایسه با طب سوزنی و سایر روشهای آرامش بخشی برای بعضی از بیماران نسبتاً مؤثر است. با این حال ، آن را کمتر از TENS و ورزش درمانی کارآمد تر است اگرچه ممکن است بیماران جداگانه یکی را ترجیح دهند. (Furlan، Andrea D.، et al.)
دستکاری ستون فقرات
این روش درمانی شامل دستکاری مفصل فراتر از حد طبیعی حرکت آن است ، اما بیشتر از حد طبیعی آناتومیک نیست. این یک روش درمانی دستی است که شامل دستکاری اهرم طولانی با سرعت پایین است. تصور می شود که کمردرد را از طریق چندین مکانیسم مانند رهاسازی اعصاب گرفتار ، تخریب چسبندگی های مفصلی و پری مفصلی و از طریق دستکاری بخش های ستون فقرات که جابجایی کرده بودند ، بهبود می بخشد. همچنین می تواند باعث کاهش شکاف دیسک ، شل شدن عضلات هیپرتونیک ، تحریک فیبرهای موضعی با تغییر عملکرد نوروفیزیولوژیک و مجدداً منیسک در سطح مفصل شود.
تصور می شود که با بیشتر روش هایی مانند TENS ، ورزش درمانی ، داروهای NSAID و درمان برگشت مدرسه ، دستکاری ستون فقرات از نظر کارآیی برتر است. تحقیقات موجود در مورد اثربخشی آن در طولانی مدت و کوتاه مدت مثبت است. همچنین استفاده از درمانگرهای تحت آموزش کمتر از مواردی که فتق دیسک و جسم شکم فقط در کمتر از یک در 1 میلیون نفر گزارش می شود ، بسیار بی خطر است. (برونفورت ، گرت ، و دیگران)
پشتیبانی کمری
بیمارانی که از کمردرد مزمن ناشی از فرآیندهای دژنراتیو در چندین سطح با چندین علت رنج می برند ممکن است از حمایت کمر بهره مند شوند. در مورد اثربخشی آن با برخی از مطالعات ادعا می شود که بهبود متوسط در تسکین فوری و بلند مدت وجود دارد ، در حالی که برخی دیگر چنین مقایسه ای را با سایر روش های درمانی نشان نمی دهند. تکیه گاه های کمر می توانند تثبیت شوند ، ناهنجاری را اصلاح کنند ، نیروهای مکانیکی را کاهش داده و حرکات ستون فقرات را محدود کنند. همچنین ممکن است به عنوان دارونما عمل کرده و درد را با ماساژ در مناطق آسیب دیده و اعمال گرما کاهش دهد.
کشش کمر
در این روش از مهار متصل به قفس الیاک و قفسه دنده تحتانی استفاده شده و برای تسکین دردهای مزمن کمر ، نیروی طولی در امتداد ستون فقرات محوری اعمال می شود. سطح و مدت نیرو مطابق بیمار تنظیم می شود و می توان آن را با استفاده از دستگاه ها هم هنگام راه رفتن و هم دراز کشیدن اندازه گیری کرد. کشش کمر با باز کردن فضاهای دیسک بین مهره ای و کاهش لوردوز کمر عمل می کند. علائم بیماری دیسک دژنراتیو به دلیل ترمیم مجدد ستون فقرات و مزایای مرتبط با آن از طریق این روش کاهش می یابد. فشرده سازی عصبی و استرس مکانیکی را برطرف می کند ، چسبندگی های موجود در جوش و ناحیه شکم و همچنین سیگنال های درد ناپسند را مختل می کند. با این وجود ، شواهد زیادی در رابطه با اثربخشی آن در کاهش درد کمر یا بهبود عملکرد روزانه وجود ندارد. علاوه بر این ، خطرات مرتبط با کشش کمری هنوز در دست بررسی است و برخی موارد گزارش شده در مواردی که باعث ایجاد فشار عصبی ، مشکلات تنفسی و فشار خون به دلیل نیروی سنگین و قرار دادن نادرست مهار شده است ، در دسترس هستند. (هارت ، آ و همکاران)
درمان پزشکی
درمان پزشکی شامل درمان دارویی با شل کننده های عضلانی ، تزریق استروئید ، NSAID ، مواد افیونی و مسکن های دیگر است. این مورد علاوه بر درمان محافظه کارانه ، در بیشتر بیماران مبتلا به دیسک دژنراتیو لازم است. دارو درمانی با هدف کنترل ناتوانی ، کاهش درد و تورم و در عین حال کیفیت زندگی بهبود یافته است. با توجه به بیمار منفرد پذیرفته می شود زیرا هیچ اجماعی در مورد درمان وجود ندارد.
آرامبخشهای عضلانی
بیماری دیسک دژنراتیو با کاهش اسپاسم عضلات و در نتیجه تسکین درد می تواند از شل کننده های عضلانی سود ببرد. اثربخشی شل کننده های عضلانی در بهبود درد و وضعیت عملکردی از طریق چندین نوع تحقیق مشخص شده است. بنزودیازپین رایج ترین شل کننده عضله در حال استفاده است.
داروهای ضد التهابی غیر استروئیدی (NSAIDs)
این داروها معمولاً به عنوان اولین قدم در بیماری دژنراسیون دیسک فراهم می کنند که ضد درد ، و همچنین اثرات ضد التهابی دارند. شواهد محکمی وجود دارد که نشان دهنده کاهش درد مزمن کمر است. اما ، استفاده از آن با اختلالات دستگاه گوارش مانند گاستریت حاد محدود است. مهار کننده های انتخابی COX2 مانند celecoxib می توانند با هدف قرار دادن گیرنده های COX2 بر این مشکل غلبه کنند. به دلیل عوارض جانبی احتمالی آن در افزایش بیماری های قلبی عروقی با مصرف طولانی مدت ، استفاده از آنها به طور گسترده ای مورد پذیرش نیست.
داروهای مخدر
این یک پله بالاتر از نردبان درد WHO است. این دارو برای بیماران مبتلا به درد شدید که به NSAID ها پاسخ نمی دهند و کسانی که دارای اختلالات غیر قابل تحمل GI با درمان NSAID هستند ، اختصاص دارد. با این حال ، تجویز مواد مخدر برای درمان کمر درد به طور قابل توجهی بین پزشکان متفاوت است. طبق ادبیات ، 3 تا 66٪ بیماران ممکن است به نوعی از مواد افیونی برای تسکین کمردرد خود استفاده کنند. حتی اگر کاهش کوتاه مدت علائم مشخص شده باشد ، خطر سو abuse مصرف طولانی مدت مواد مخدر ، میزان بالای تحمل و ناراحتی تنفسی در افراد مسن وجود دارد. تهوع و استفراغ برخی از عوارض جانبی کوتاه مدت است که با آنها روبرو می شود. (Review بررسی سیستماتیک: درمان مواد افیونی برای درد مزمن کمر: شیوع ، اثر بخشی و ارتباط با اعتیاد)
ضد افسردگی
ضد افسردگی ها ، در دوزهای پایین ، ارزش ضد درد دارند و ممکن است در بیماران کمردرد مزمن که ممکن است با علائم افسردگی همراه باشند ، مفید باشد. درد و رنج ممکن است باعث اختلال در خواب بیمار و کاهش آستانه درد شود. این موارد را می توان با استفاده از داروهای ضد افسردگی در دوزهای پایین مرتفع کرد ، حتی اگر هیچ مدرکی مبنی بر بهبود عملکرد وجود نداشته باشد.
تزریق درمانی
تزریق استروئید اپیدورال
تزریق استروئید اپیدورال پرمصرف ترین نوع تزریق برای درمان بیماری مزمن دیسژنزای مزمن و رادیکولوپاتی همراه است. بین نوع استروئید مورد استفاده و دوز آن تفاوت وجود دارد. 8- 10 میلی لیتر از مخلوط متیل پردنیزولون و نرمال سالین یک دوز موثر و بی خطر در نظر گرفته می شود. تزریق را می توان از طریق مسیرهای interlaminar ، caudal یا trans-foramina انجام داد. سوزن را می توان تحت هدایت فلوروسکوپی وارد کرد. کنتراست اول ، سپس بی حسی موضعی و در آخر ، استروئید از طریق این روش به فضای اپیدورال در سطح آسیب دیده تزریق می شود. تسکین درد به دلیل ترکیبی از اثرات هر دو بی حسی موضعی و استروئید حاصل می شود. تسکین فوری درد از طریق بی حسی موضعی با مسدود کردن انتقال سیگنال درد و در عین حال تأیید تشخیص نیز حاصل می شود. التهاب نیز به دلیل عمل استروئیدها در مسدود کردن آبشار پیش التهابی کاهش می یابد.
در طی دهه اخیر ، استفاده از تزریق استروئید اپیدورال 121٪ افزایش یافته است. با این حال ، در مورد استفاده از آن به دلیل تغییر در سطح پاسخ و عوارض جانبی بالقوه جدی ، اختلاف نظر وجود دارد. معمولاً اعتقاد بر این است که این تزریق ها فقط باعث تسکین علائم در کوتاه مدت می شوند. برخی از پزشکان ممکن است در مدت یک هفته 2 تا 3 آمپول تزریق کنند ، اگرچه نتایج دراز مدت برای یک بیمار که فقط یک بار تزریق می شود یکسان است. برای یک دوره یک ساله ، نباید بیش از 4 آمپول تزریق شود. برای تسکین فوری و موثرتر درد ، می توان مورفین بدون مواد نگهدارنده را نیز به تزریق افزود. برای این منظور حتی بی حس کننده های موضعی مانند لیدوکائین و بوپیواکائین نیز اضافه می شوند. شواهد مربوط به تسکین درد طولانی مدت محدود است. ("یک آزمایش کنترل شده با دارونما برای ارزیابی اثر تسکین درد با استفاده از کتامین با استروئیدهای اپیدورال برای کمردرد مزمن")
علاوه بر نگرانی های بالای هزینه و کارآیی ، به دلیل این روش درمانی عوارض جانبی بالقوه ای نیز دارد. در صورت عدم استفاده از فلوروسکوپی در 25٪ موارد ، حتی با حضور پرسنل باتجربه ، سوزنها می توانند بیجا شوند. محل قرارگیری اپیدورال را می توان با خارش قابل اطمینان تشخیص داد. تنفس تنفسی یا احتباس ادرار می تواند به دنبال تزریق مورفین اتفاق بیفتد ، بنابراین بیمار باید 24 ساعت پس از تزریق تحت نظر قرار گیرد.
تزریق های صورت
این تزریقات به اتصالات مفاصل صورت داده می شود ، همچنین به آنها مفاصل زیگاپوفیزیال گفته می شود که بین دو مهره مجاور قرار دارند. بیهوشی را می توان مستقیماً به فضای مفصل یا به شاخه داخلی مرتبط با رمی خلفی تزریق کرد که آن را درونی می کند. شواهدی وجود دارد که نشان می دهد این روش توانایی عملکردی ، کیفیت زندگی را بهبود می بخشد و درد را تسکین می بخشد. تصور می شود که اینها مزایای کوتاه مدت و بلند مدت را ارائه می دهند ، اگرچه مطالعات نشان داده اند که تزریق های صورت و تزریق استروئید اپیدورال از نظر کارایی مشابه هستند. (وین ، کلی الف)
تزریقات مشترک SI
این یک مفصل سینوویال دیارترودیال با تأمین اعصاب از هر دو آکسون عصبی میلین و غیر میلین است. این تزریق می تواند بیماری دیسک دژنراتیو را که شامل مفصل ساکروایلیاک می شود ، درمان کند و منجر به تسکین طولانی مدت و کوتاه مدت از علائمی مانند کمردرد و درد درد در پاها ، ران و باسن شود. تزریق هر 2 تا 3 ماه می تواند تکرار شود اما فقط در صورت لزوم بالینی باید انجام شود. (MAUGARS، Y. et al.)�
روشهای درمانی غیر عملی برای درد دیسکوژنیک
همانطور که در تحقیقات ذکر شده است ، دیسکوگرافی هم به عنوان روشی تشخیصی و درمانی قابل استفاده است. بعد از شناسایی دیسک بیمار ، می توان چندین روش با حداقل تهاجمی را قبل از شروع عمل جراحی امتحان کرد. از جریان الکتریکی و گرمای آن می توان برای انعقاد انسداد خلفی در نتیجه تقویت فیبرهای کلاژن ، تغییر شکل دهنده و از بین بردن واسطه ها و گیرنده های التهابی و مهر و موم کردن استفاده کرد. روشهای مورد استفاده در این روش ، نامشخصی درمانی داخلی (IDET) یا آنالوپلاستی خلفی خلفی رادیویی (RFET) است که در آن یک الکترود به دیسک منتقل می شود. IDET شواهد متوسطی در زمینه تسکین علائم برای بیماران مبتلا به بیماری دژنراسیون دیسک دارد ، در حالی که حزب کمونیست از نظر اثر بخشی کوتاه مدت و طولانی مدت از حمایت محدودی برخوردار است. هر دو روش ممکن است منجر به عوارضی مانند آسیب ریشه عصبی ، نقص عملکرد سوند ، عفونت و فتق دیسک بعد از عمل شود.
درمان جراحی
درمان جراحی برای بیماران با درمان محافظه کارانه ناموفق با در نظر گرفتن شدت بیماری ، سن ، سایر بیماری های همراه ، شرایط اقتصادی - اجتماعی و سطح نتیجه مورد انتظار اختصاص دارد. تخمین زده می شود که حدود 5٪ از بیماران مبتلا به دیسک تحلیل برنده تحت عمل جراحی قرار می گیرند ، چه به دلیل بیماری کمر و چه به دلیل گردن رحم. (Rydevik ، Bj rn L.)
روش های ستون فقرات کمر
جراحی کمر در بیماران با درد شدید ، با مدت زمان 6 تا 12 ماه درمان دارویی بی اثر ، که دارای تنگی حسی مهم در ستون فقرات هستند ، نشان داده می شود. جراحی معمولاً یک روش انتخابی است به جز در مورد سندرم cauda equina. دو نوع روش وجود دارد که هدف آنها شامل همجوشی ستون فقرات یا رفع فشار یا هر دو است. (e بیماری دیسک دژنراتیو: زمینه ، آناتومی ، پاتوفیزیولوژی. )
همجوشی ستون فقرات شامل متوقف کردن حرکات در یک قسمت مهره دردناک به منظور کاهش درد با همجوشی چندین مهره به هم با استفاده از پیوند استخوانی است. این در دراز مدت برای بیماران مبتلا به بیماری دیسک انحطاطی که دارای بدخیمی ستون فقرات یا حرکت بیش از حد هستند ، مؤثر تلقی می شود. روش های مختلفی برای جراحی فیوژن وجود دارد. (گوپتا ، ویجی کومار و همکاران)
- همجوشی روده خلفی ستون فقرات کمر
این روش شامل قرار دادن پیوند استخوانی در قسمت خلفی ستون فقرات است. پیوند استخوان را می توان از تاج ایلیاک خلفی برداشت کرد. استخوانها برای پیوند موفقیت آمیز از پیستونی آن جدا می شوند. در دوره بعد از عمل نیاز به بریس پشتی وجود دارد و بیماران ممکن است نیاز داشته باشند حدود 5 تا 10 روز در بیمارستان بمانند. حرکات محدود و ترک سیگار برای فیوژن موفقیت آمیز مورد نیاز است. با این وجود ، خطرات مختلفی از قبیل عدم اتحاد ، عفونت ، خونریزی و اتحاد جامد با کمردرد ممکن است رخ دهد.
- همجوشی کمر خلفی خلفی
در این روش ، روش های رفع فشار یا دیسککتومی نیز با همان رویکرد قابل انجام است. پیوند استخوان مستقیماً در فضای دیسک اعمال می شود و لیگامنت فلاوم کاملاً خارج می شود. برای بیماری دیسک دژنراتیو ، فضای بین لمینار علاوه بر این با انجام یک اکتسکتومی میانی جزئی نیز گسترش می یابد. بریس های عقب با این روش اختیاری هستند. در مقایسه با روش قدامی ، فقط معایب آن وجود دارد ، از جمله اینکه فقط می توان پیوندهای کوچکی در نظر گرفت ، کاهش سطح موجود برای همجوشی و مشکل در هنگام انجام عمل جراحی بر روی بیماران مبتلا به ناهنجاری نخاعی. مهمترین خطر این عدم اتحادیه است.
- همجوشی متقابل کمر قدامی
این روش مشابه با خلفی است به جز اینکه از طریق شکم به جای پشت به آن نزدیک می شود. این مزیت را دارد که باعث اختلال در عضلات کمر و تامین عصب نمی شود. این بیماری در بیماران مبتلا به پوکی استخوان منع مصرف دارد و خطر خونریزی ، انزال رتروگراد در مردان ، عدم اتحادیه و عفونت را دارد.
- ترانسفورمینال همجوشی کمری
این یک نسخه اصلاح شده از رویکرد خلفی است که در حال محبوبیت است. با قرار گرفتن در معرض خوب ، خطر کمتری را به همراه دارد و نشان داده می شود که با چند عارضه مانند نشت CSF ، اختلال عصبی گذرا و عفونت زخم نتیجه بسیار خوبی دارد.
آرتروپلاستی کامل دیسک
این یک جایگزین برای همجوشی دیسک است و از آن برای درمان بیماری دیسک دژنراسیون کمری با استفاده از یک دیسک مصنوعی برای جایگزینی دیسک آسیب دیده استفاده شده است. پروتز كل یا پروتز هسته ای بسته به وضعیت بالینی می تواند مورد استفاده قرار گیرد.
فشرده سازی شامل از بین بردن قسمتی از دیسک بدن مهره است که برای رهایی آن عصبی ایجاد می شود و از طریق روش هایی به نام دیسککتومی و لامینکتومی فضای بهبودی آن را فراهم می کند. کارآیی این روش اگرچه یک عمل جراحی معمول است ، جای سوال دارد. عوارض بسیار کمی با احتمال کم عود علائم با رضایت بیمار بیشتر است. (گوپتا ، ویجی کومار و همکاران)
- دیسککتومی کمری
این عمل جراحی از طریق یک روش خط میانی خلفی با تقسیم آهسته لیگامان انجام می شود. ریشه عصبی که تحت تأثیر قرار گرفته شناسایی شده و برای آزاد شدن آن ، حلقه برآمده بریده می شود. معاینه عصبی کامل باید بعد از آن انجام شود و بیماران معمولاً 1 تا 5 روز بعد می توانند به خانه بروند. تمرینات کمر باید به زودی شروع شود و به دنبال آن کار سبک و سپس کار سنگین به ترتیب در 2 و 12 هفته انجام شود.
- لامینکتومی کمر
این روش می تواند کاملاً یک سطح و همچنین از طریق چندین سطح انجام شود. لامینکتومی باید تا حد امکان کوتاه باشد تا از بی ثباتی ستون فقرات جلوگیری شود. به دنبال این عمل ، بیماران علائم و کاهش رادیکولوپاتی را کاهش داده اند. خطرات ممکن است شامل بی اختیاری روده و مثانه ، نشت CSF ، آسیب ریشه عصبی و عفونت باشد.
روشهای ستون فقرات گردن رحم
در صورت وجود درد غیر قابل تحمل همراه با نقص حرکتی پیشرونده و حسی ، بیماری دیسک تخریب گردن رحم برای جراحی نشان داده می شود. هنگامی که شواهد رادیوگرافیکی از فشرده سازی ریشه عصب وجود دارد ، نتیجه جراحی بیش از 90٪ است. چندین گزینه وجود دارد از جمله دیسککتومی گردن قدامی (ACD) ، ACD و همجوشی (ACDF) ، ACDF با تثبیت داخلی و فروامینوتومی خلفی. (e بیماری دیسک دژنراتیو: زمینه ، آناتومی ، پاتوفیزیولوژی. )
درمان مبتنی بر سلول
پیوند سلول های بنیادی به عنوان یک درمان جدید برای بیماری دیسک دژنراتیو با نتایج امیدوارکننده پدید آمده است. معرفی سلولهای غضروفی اتولوگ برای کاهش درد discogenic در طی یک دوره 2 ساله یافت شده است. این روشهای درمانی در حال حاضر تحت آزمایشهای انسانی قرار دارند. (جئونگ ، جون هون و دیگران)
ژن درمانی
انتقال ژن به منظور متوقف کردن روند تخریب دیسک و حتی القای احیای دیسک در حال حاضر تحت بررسی است. برای این کار ، باید با استفاده از فعالیتهای ژنهای تقویت کننده انحطاط ، ژنهای مفید شناسایی شود. این گزینه های جدید درمانی ، امید به درمان آینده برای بازسازی دیسک های بین مهره ای دارند. (نیشیدا ، کوتارو و دیگران)

بیماری دیسک دژنراتیو یک مسئله بهداشتی است که با کمردرد مزمن ناشی از دیسک بین مهره آسیب دیده مانند کمردرد در ستون فقرات کمری یا گردن در گردن رحم ایجاد می شود. این یک شکستگی دیسک بین مهره ای ستون فقرات است. چندین تغییر پاتولوژیک در تخریب دیسک ممکن است رخ دهد. نقایص آناتومیکی مختلف نیز در دیسک بین مهره ای ایجاد می شود. کمردرد و درد گردن از مشکلات عمده اپیدمیولوژیک است که تصور می شود مربوط به بیماری دیسک دژنراتیو است. کمردرد دومین علت اصلی مراجعه به مطب پزشکان در ایالات متحده است. تخمین زده می شود که حدود 80٪ از بزرگسالان آمریکایی حداقل یک بار در طول زندگی خود از کمردرد رنج می برند. بنابراین ، درک کامل از بیماری دیسک دژنراتیو برای مدیریت این بیماری مشترک لازم است. - دکتر الکس جیمنز DC ، CCST Insight
دامنه اطلاعات ما محدود به کایروپراکتیک ، اسکلت عضلانی ، داروهای فیزیکی ، سلامتی و مسائل حساس بهداشتی و / یا مقالات ، موضوعات و مباحث مربوط به پزشکی کاربردی است. ما برای درمان و پشتیبانی از مراقبت از آسیب ها یا اختلالات سیستم اسکلتی عضلانی از پروتکل های سلامتی و تندرستی استفاده می کنیم. پست ها ، موضوعات ، موضوعات و بینش های ما شامل موارد کلینیکی ، موضوعات و موضوعاتی است که به طور مستقیم یا غیرمستقیم دامنه عملکرد بالینی ما رابط و پشتیبانی می کند. * دفتر ما تلاش معقولانه ای برای ارائه استنادات حمایتی انجام داده و مطالعه تحقیقاتی مرتبط مطالعات پشتیبانی از پست های ما ما همچنین کپی از مطالعات تحقیقاتی پشتیبانی را در صورت درخواست در دسترس هیئت مدیره و یا مردم قرار می دهیم. ما درک می کنیم که مواردی را که نیاز به توضیح اضافی در مورد چگونگی کمک به آن در یک برنامه مراقبت خاص یا پروتکل درمان دارند ، پوشش می دهیم. بنابراین ، برای بحث بیشتر در مورد موضوع بالا ، لطفا در صورت تمایل از دکتر الکس خیمنز بپرسید یا با ما تماس بگیرید 915-850-0900. ارائه دهنده (ها) دارای مجوز در تگزاس * و نیومکزیکو *
طراحی شده توسط دکتر الکس Jimenez DC ، CCST
منابع
- �بیماری دژنراتیو دیسک.� Spine-Health، 2017، www.spine-health.com/glossary/degenerative-disk-sease.
- مودیچ ، مایکل تی و جفری اس راس. بیماری دیسک انحطاطی کمری. رادیولوژی ، جلد 245 ، شماره. 1 ، 2007 ، صص 43-61. انجمن رادیولوژی آمریکای شمالی (RSNA) ، doi: 10.1148 / radiol.2451051706.
- بیماری دژنراتیو دیسک: زمینه، آناتومی، پاتوفیزیولوژی. Emedicine.Medscape.Com، 2017، emedicine.medscape.com/article/1265453-overview.
- طاهر ، فادی و دیگران. Disc بیماری دیسک انحطاطی کمر: مفاهیم کنونی و آینده تشخیص و مدیریت. پیشرفت در ارتوپدی ، جلد 2012 ، 2012 ، صص 1-7. Hindawi Limited ، doi: 10.1155 / 2012/970752.
- چوی ، یونگ سو athپاتوفیزیولوژی بیماری دیسک دژنراتیو. مجله آسیایی ستون فقرات ، جلد 3 ، شماره. 1 ، 2009 ، ص. 39. انجمن جراحی ستون فقرات کره (KAMJE) ، doi: 10.4184 / asj.2009.3.1.39.
- واتر ، پل آر و همکاران بافت شناسی عملکردی Wheater. چاپ پنجم ، [دهلی نو] ، چرچیل لیوینگستون ، 5 ،.
- پالمگرن ، توو و همکاران Imبررسی ایمونوهیستوشیمیایی ساختارهای عصبی در آنبول فیبروسوس دیسکهای بین مهره ای کمر طبیعی انسان. ستون فقرات ، جلد 24 ، شماره. 20 ، 1999 ، ص. 2075. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.1097 / 00007632-199910150-00002.
- BOGDUK ، NIKOLAI و همکاران nerنوشناختی دیسک های بین مهره ای گردنی. ستون فقرات ، جلد 13 ، شماره. 1 ، 1988 ، صص 2-8. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.1097 / 00007632-198801000-00002.
- �دیسک بین مهره ای � ستون فقرات � Orthobullets.Com. Orthobullets.Com، 2017، www.orthobullets.com/spine/9020/intervertebral-disc.
- سوتار ، پوخراج. ارزیابی MRI از بیماری دژنراتیو دیسک کمر. مجله تحقیقات بالینی و تشخیصی ، 2015 ، تحقیقات و انتشارات JCDR ، doi: 10.7860 / jcdr / 2015 / 11927.5761.
- باکوالتر ، جوزف آ. «پیری و انحطاط دیسک بین مهره ای انسان» ستون فقرات ، جلد 20 ، شماره. 11 ، 1995 ، صص 1307-1314. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.1097 / 00007632-199506000-00022.
- رابرتز ، S. و همکاران «پیری در دیسک های بین مهره ای انسان». European Spine Journal، جلد 15، شماره. S3 ، 2006 ، صص 312-316. Springer Nature ، doi: 10.1007 / s00586-006-0126-8.
- Boyd ، Lawrence M. et al. De تخریب زودرس دیسک بین مهره ای و صفحه انتهایی مهره در موش های دارای کمبود نوع کلاژن نوع IX. آرتروز و روماتیسم ، جلد 58 ، شماره. 1 ، 2007 ، صص 164-171. ویلی-بلک ول ، doi: 10.1002 / art.23231.
- ویلیامز ، FMK ، و PN سامبروک. Pain گردن و کمر درد و انحطاط دیسک بین مهره ای: نقش عوامل شغلی. بهترین تمرین و تحقیقات روماتولوژی بالینی ، جلد 25 ، شماره. 1 ، 2011 ، ص 69-79. Elsevier BV ، doi: 10.1016 / j.berh.2011.01.007.
- Batti ، Michele C. De تحلیل رفتن دیسک کمر: اپیدمیولوژی و ژنتیک. مجله جراحی استخوان و مفصل (آمریکایی) ، جلد 88 ، شماره. suppl_2 ، 2006 ، ص. 3. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.2106 / jbjs.e.01313.
- BATTI ، MICHELE C. و همکاران Award1991 جایزه ولوو در علوم بالینی. ستون فقرات ، جلد 16 ، شماره. 9 ، 1991 ، صص 1015-1021. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.1097 / 00007632-199109000-00001.
- Kauppila، LI tآترواسکلروز و انحطاط دیسک / کمردرد یک بررسی سیستماتیک. مجله جراحی عروق ، جلد 49 ، شماره. 6 ، 2009 ، ص. 1629. Elsevier BV ، doi: 10.1016 / j.jvs.2009.04.030.
- Stud یک مطالعه مبتنی بر جمعیت ، از انحطاط دیسک نوجوانان و ارتباط آن با اضافه وزن و چاقی ، کمردرد و کاهش عملکرد. Samartzis D ، Karppinen J ، Mok F ، Fong DY ، Luk KD ، Cheung KM. J Bone Joint Surg Am 2011؛ 93 (7): 662 70. مجله ستون فقرات ، جلد 11 ، شماره. 7 ، 2011 ، ص. 677. Elsevier BV ، doi: 10.1016 / j.spinee.2011.07.008.
- گوپتا ، ویجی کومار و دیگران. Disc بیماری دیسک دژنراتیو کمر: رویکردهای ارائه و درمان بالینی. Journal مجله IOSR علوم دندانپزشکی و پزشکی ، سال 15 ، شماره. 08 ، 2016 ، صص 12-23. مجلات IOSR ، doi: 10.9790 / 0853-1508051223.
- باتناگار ، سوشما و میناک گوپتا. Gu رهنمودهای عملی بالینی مبتنی بر شواهد برای مدیریت درد مداخله ای در درد سرطان. Journal مجله هند مراقبت از تسکین ، جلد 21 ، شماره. 2 ، 2015 ، ص. 137. Medknow ، doi: 10.4103 / 0973-1075.156466.
- KIRKALDY-WILLIS ، WH و همکاران athپاتولوژی و پاتوژنز اسپوندیلوز کمر و تنگی. ستون فقرات ، جلد 3 ، شماره. 4 ، 1978 ، صص 319-328. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.1097 / 00007632-197812000-00004.
- KONTTINEN ، YRJ T. و دیگران. eتحلیل عصبی ایمونوهیستوشیمی عناصر عصبی درد پری دیسکال. ستون فقرات ، جلد 15 ، شماره. 5 ، 1990 ، صص 383-386. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.1097 / 00007632-199005000-00008.
- بریزبی ، هلنا آسیب شناسی و مکانیسم های احتمالی پاسخ سیستم عصبی به انحطاط دیسک. مجله جراحی استخوان و مفصل (آمریکایی) ، جلد 88 ، شماره. suppl_2 ، 2006 ، ص. 68. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.2106 / jbjs.e.01282.
- جیسون ام. هایسمیت، MD. �علائم بیماری دژنراتیو دیسک | کمر درد، درد پا. Spineuniverse، 2017، www.spineuniverse.com/conditions/degenerative-disc/symptoms-degenerative-disc-sease.
- �بیماری دژنراتیو دیسک � فیزیوپدی. Physio-Pedia.Com، 2017، www.physio-pedia.com/Degenerative_Disc Disease.
- Modic ، MT و همکاران eبیماری دیژنراتیو دیسک: ارزیابی تغییرات در مغز مهره های بدن با تصویربرداری MR.. vol رادیولوژی ، جلد 166 ، شماره. 1 ، 1988 ، صص 193-199. انجمن رادیولوژی آمریکای شمالی (RSNA) ، doi: 10.1148 / radiology.166.1.3336678.
- Pfirrmann ، Christian WA و همکاران Class طبقه بندی تشدید مغناطیسی تخریب دیسک بین مهره ای کمر. ستون فقرات ، جلد 26 ، شماره. 17 ، 2001 ، ص 1873-1878. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.1097 / 00007632-200109010-00011.
- بارتینسکی ، والتر اس. و ا. اورلاندو اورتیز. nt ارزیابی متداول دیسک کمر: دیسکوگرافی کمری تحریک و دیسکوگرافی بیهوشی عملکردی. تکنیک ها در رادیولوژی عروقی و مداخله ای ، جلد 12 ، شماره. 1 ، 2009 ، صص 33-43. Elsevier BV ، doi: 10.1053 / j.tvir.2009.06.003.
- Narouze ، Samer و Ameresh Vydyanathan. تزریق ترانسفورامینال دهانه رحم با سونوگرافی و بلوک ریشه اعصاب انتخابی. تکنیک های بیهوشی منطقه ای و مدیریت درد ، جلد 13 ، شماره. 3 ، 2009 ، صص 137-141. Elsevier BV ، doi: 10.1053 / j.trap.2009.06.016.
- ournal ژورنال تقویم الکترومیوگرافی و حرکت شناسی. مجله الکترومیوگرافی و حرکت شناسی ، جلد 4 ، شماره. 2 ، 1994 ، ص. 126. Elsevier BV ، doi: 10.1016 / 1050-6411 (94) 90034-5.
- Hayden ، Jill A. و همکاران Review بررسی سیستماتیک: راهکارهای استفاده از ورزش درمانی برای بهبود نتایج در کمر درد مزمن. Annals Of Internal Medicine، جلد 142، شماره. 9 ، 2005 ، ص. 776. کالج پزشکان آمریکا ، doi: 10.7326 / 0003-4819-142-9-200505030-00014.
- جانسون ، مارک I. St تحریک الکتریکی اعصاب از طریق پوست (TENS) و دستگاههایی مانند TENS: آیا آنها تسکین دهنده درد هستند؟. Reviews بررسیهای درد ، جلد 8 ، شماره. 3-4 ، 2001 ، صص 121-158. رواق ، doi: 10.1191 / 0968130201pr182ra.
- هارت ، ا و همکاران اثر کشش کمر در کنترل کمردرد. فیزیوتراپی ، جلد 88 ، شماره. 7 ، 2002 ، ص 433-434. Elsevier BV ، doi: 10.1016 / s0031-9406 (05) 61278-3.
- برونفورت ، گرت و همکاران اثر دستکاری و تحرک ستون فقرات برای کمردرد و گردن درد: یک مرور سیستماتیک و بهترین سنتز شواهد. مجله ستون فقرات ، جلد 4 ، شماره. 3 ، 2004 ، صص 335-356. Elsevier BV ، doi: 10.1016 / j.spinee.2003.06.002.
- Furlan ، Andrea D. و دیگران assماساژ برای کمردرد: یک مرور سیستماتیک در چارچوب گروه بررسی مجدد همکاری کوکرین. ستون فقرات ، جلد 27 ، شماره. 17 ، 2002 ، ص 1896-1910. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.1097 / 00007632-200209010-00017.
- Review بررسی سیستماتیک: درمان با مواد افیونی برای درد مزمن کمر: شیوع ، اثر بخشی و ارتباط با اعتیاد. Govern حکمرانی بالینی: یک مجله بین المللی ، جلد 12 ، شماره. 4 ، 2007 ، زمرد ، doi: 10.1108 / cgij.2007.24812dae.007.
- کارآزمایی کنترل شده با دارونما برای ارزیابی تأثیر تسکین درد با استفاده از کتامین با استروئیدهای اپیدورال برای کمردرد مزمن. مجله بین المللی علوم و تحقیقات (IJSR) ، جلد 5 ، شماره. 2 ، 2016 ، ص 546-548. مجله بین المللی علوم و تحقیقات ، doi: 10.21275 / v5i2.nov161215.
- Wynne، Kelly A. تزریقات مفصلی در مدیریت مزمن کمردرد: مروری. بررسی درد ، جلد 9 ، شماره. 2 ، 2002 ، صص 81-86. رواق ، doi: 10.1191 / 0968130202pr190ra.
- MAUGARS ، Y. و دیگران ارزیابی اثرات تزریق کورتیکواستروئید ساکرولیلیاک در اسپروتروپاتی ها: یک مطالعه دو سو کور. روماتولوژی ، جلد 35 ، شماره. 8 ، 1996 ، صص 767-770. انتشارات دانشگاه آکسفورد (OUP) ، doi: 10.1093 / rheumatology / 35.8.767.
- Rydevik، Bj rn L. oنظر نقطه نظر: نتیجه هفت تا 10 ساله جراحی افت فشار برای تنگی استخوان ستون فقرات کمری دژنراتیو. ستون فقرات ، جلد 21 ، شماره. 1 ، 1996 ، ص. 98. Ovid Technologies (Wolters Kluwer Health) ، doi: 10.1097 / 00007632-199601010-00023.
- جئونگ ، جی هون و دیگران e بازسازی دیسک های بین مهره ای در یک مدل تخریب دیسک موش صحرایی توسط سلولهای استرومایی استخراج شده از بافت چربی-کاشته شده. 152 ، 10 ، صص 2010-1771. Springer Nature ، doi: 1777 / s10.1007-00701-010-0698.
- نیشیدا ، کوتارو و دیگران. رویکرد ژن درمانی برای تخریب دیسک و اختلالات مرتبط با ستون فقرات. European Spine Journal، جلد 17، شماره. S4 ، 2008 ، صص 459-466. Springer Nature ، doi: 10.1007 / s00586-008-0751-5.
اطلاعات اینجا در "بیماری دیسک دژنراتیو (DDD) چیست؟: یک مرور کلی"در نظر گرفته شده است که جایگزین رابطه یک به یک با یک متخصص مراقبت های بهداشتی واجد شرایط یا پزشک دارای مجوز نیست و توصیه پزشکی نیست. ما شما را تشویق می کنیم که تصمیمات مراقبت های بهداشتی را بر اساس تحقیقات و مشارکت خود با یک متخصص مراقبت های بهداشتی واجد شرایط اتخاذ کنید.
محدوده اطلاعاتی ما محدود به کایروپراکتیک، اسکلتی عضلانی، داروهای فیزیکی، سلامتی، کمک کننده به علت اختلالات احشایی در ارائه های بالینی، پویایی بالینی رفلکس سوماتوویسرال مرتبط، کمپلکس های سابلوکساسیون، مسائل حساس سلامتی، و/یا مقالات، موضوعات و بحث های پزشکی کاربردی.
ارائه و ارائه می کنیم همکاری بالینی با متخصصین رشته های مختلف هر متخصص بر اساس حوزه فعالیت حرفه ای و صلاحیت مجوز آنها اداره می شود. ما از پروتکل های عملکردی سلامت و تندرستی برای درمان و حمایت از مراقبت از آسیب ها یا اختلالات سیستم اسکلتی عضلانی استفاده می کنیم.
ویدیوها، پستها، موضوعات، موضوعات و بینشهای ما، موضوعات، مسائل و موضوعات بالینی را پوشش میدهد که به طور مستقیم یا غیرمستقیم به حوزه عمل بالینی ما مربوط میشود و به طور مستقیم یا غیرمستقیم از آن پشتیبانی میکند.*
دفتر ما به طور منطقی تلاش کرده است تا استنادات حمایتی ارائه دهد و مطالعه تحقیقاتی یا مطالعات مرتبط با پست های ما را شناسایی کرده است. ما کپی از مطالعات تحقیقاتی پشتیبانی را که در صورت درخواست در دسترس هیئت های نظارت و عموم است ، ارائه می دهیم.
ما می فهمیم که مواردی را پوشش می دهیم که نیاز به توضیح اضافی در مورد چگونگی کمک به آن در یک برنامه مراقبت خاص یا پروتکل درمانی دارند. بنابراین ، برای بحث بیشتر در مورد موضوع فوق ، لطفاً آزادانه س .ال کنید دکتر الکس جیمنز، دی سی, و یا با ما تماس بگیرید در 915-850-0900.
ما برای کمک به شما و خانواده شما اینجا هستیم.
نعمت
دکتر الکس جیمنز DC ، MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
ایمیل شما: coach@elpasofunctionalmedicine.com
دارای مجوز به عنوان دکتر کایروپراکتیک (DC) در وابسته به تکزاس & نیومکزیکو*
مجوز تگزاس دی سی شماره TX5807, نیومکزیکو دی سی مجوز # NM-DC2182
دارای مجوز به عنوان پرستار ثبت شده (RN*) in فلوریدا
مجوز RN مجوز فلوریدا # RN9617241 (شماره کنترل 3558029)
وضعیت فشرده: مجوز چند ایالتی: مجاز به تمرین در کشورهای 40*
دکتر الکس جیمنز DC، MSACP، RN* CIFM*، IFMCP*، ATN*، CCST
کارت ویزیت دیجیتال من