مکانیسم های مسیر مدولاسیون درد در ال پاسو، TX
اغلب، اگر نه همه، بیماری های بدن باعث درد می شود. درد در مغز تفسیر و حس می شود. درد توسط دو نوع کلیدی از مواد مخدر که بر روی مغز کار می کنند، مدوله می شود: ضد درد و بیهوشی. اصطلاح ضد درد به دارویی اطلاق می شود که درد را بدون از دست دادن آگاهی از بین می برد. بیهوشی مرکزی بیانگر داروهایی است که CNS را مهار می کند. این به دلیل فقدان همه ادراکات حالت های حسی، به عنوان مثال، از دست دادن آگاهی بدون از دست دادن توابع بحرانی مشخص می شود.
اپیدمی آنژژی (OA)
موفق ترین داروهای مورد استفاده بالینی برای تولید موضعی ضد درد و تسکین درد، خانواده های مخدر هستند که شامل مورفین و هرویین هستند. در حال حاضر گزینه های دیگری برای مبارزه با درد درمانی قوی وجود ندارد. چندین عوارض ناشی از مصرف مواد مخدر شامل تحمل و وابستگی به مواد یا اعتیاد هستند. به طور کلی، این داروها اطلاعات درد ناشی از درد در ستون فقرات و سیستم عصبی مرکزی را مد نظر قرار می دهد، علاوه بر اینکه درد را به طور موقت از بین می برد، و همچنین می تواند به عنوان داروهای ضدافسردگی تولید مثل (OA) نام برد. آنتاگونیست Opiate داروهایی است که اثرات مهاری نظیر نالوکسون یا مالتروکسون و غیره را در مقابل آن قرار می دهد. آنها آنتاگونیست های رقابتی گیرنده های اپیت هستند. با این حال، مغز یک مدار عصبی و مواد درونی دارد که درد را تعدیل می کند.
اپیوئیدهای اندوژن
انتقال عصبی اپوئیدرژیک در سراسر مغز و نخاع قرار دارد و اعتقاد بر این است که بسیاری از توابع سیستم عصبی مرکزی یا CNS را تحت تاثیر قرار می دهد، از قبیل نوکسیپس، توابع قلب و عروق، تنظیم حرارت، تنفس، عملکردهای نورولوژیک، تومورهای عصبی، مصرف مواد غذایی، فعالیت جنسی، رقابتی رفتار حرکتی و حافظه و یادگیری. اوپیوئید ها تأثیرات مشخصی روی خلق و خوی و انگیزه ایجاد می کنند و موجب ایجاد ناخوشایند می شوند.
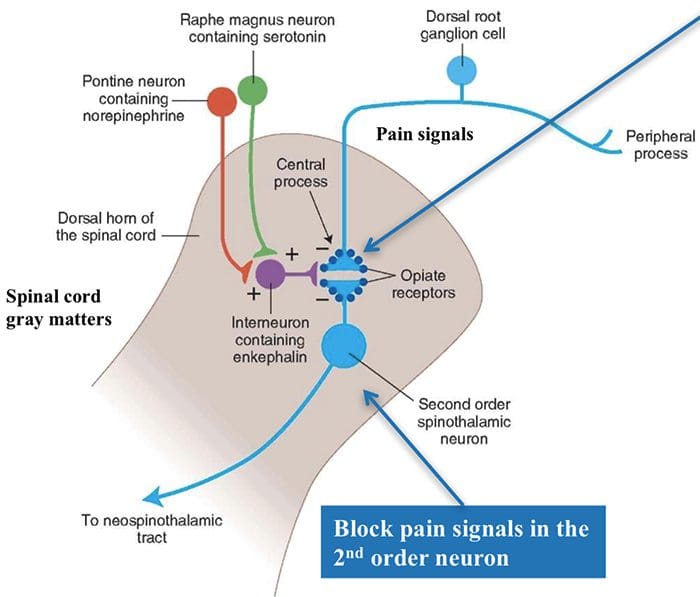
سه دسته از گیرنده های اپیوئیدی شناسایی می شوند: β-mu، β-دلتا و β-کاپا. هر 3 کلاس به طور گسترده در مغز پراکنده هستند. ژنهای کدکننده هر یک از این ژنها شبیهسازی شدهاند و به عنوان اعضای گیرندههای پروتئین G عمل میکنند. علاوه بر این، سه نوع عمده از پپتیدهای شبه افیونی درون زا که با گیرنده های مواد افیونی فوق در تعامل هستند، در سیستم عصبی مرکزی شناسایی شده اند، از جمله، β-اندورفین ها، انکفالین ها و دینورفین ها. این 3 پپتید اپیوئیدی از یک گیرنده پروتئینی بزرگ توسط سه ژن مختلف مشتق شده اند، مانند ژن proopiomelanocortin یا POMC، ژن proenkephalin و ژن prodynorphin. پپتیدهای اپیوئیدی ورودی درد را به دو طریق تعدیل می کنند: اول اینکه انتقال دهنده های عصبی را مسدود می کنند. با مهار هجوم Ca2+ به پایانه پیش سیناپسی آزاد می شوند، یا ثانیاً کانال های پتاسیم را باز می کنند که نورون ها را هیپرپلاریزه کرده و فعالیت اسپایک را مهار می کند. آنها بر روی گیرنده های مختلف در مغز و نخاع عمل می کنند.
انکفالین ها لیگاندهای احتمالی برای ? گیرنده ها، اندورفین برای گیرنده های ? و دینورفین برای گیرنده های ? گیرنده ها انواع مختلف گیرنده های اپیوئیدی به طور متفاوتی در سیستم عصبی محیطی و مرکزی یا CNS توزیع می شوند. شواهدی مبنی بر تفاوت های عملکردی در این گیرنده ها در ساختارهای مختلف وجود دارد. این توضیح می دهد که چرا بسیاری از عوارض جانبی نامطلوب پس از درمان با مواد افیونی رخ می دهد. برای مثال، گیرندههای مو (؟) در هستههای پارابراکیال ساقهی مغز گسترده هستند، جایی که یک مرکز تنفسی و مهار این نورونها ممکن است باعث آنچه به عنوان افسردگی تنفسی شناخته میشود، شود.
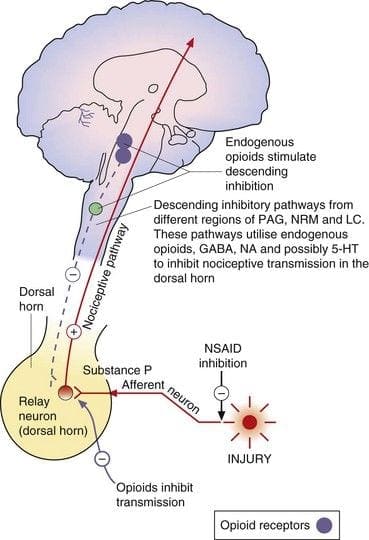
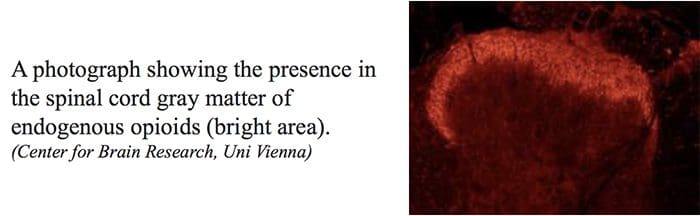
پایانه های مرکزی یا محیطی فیبرهای آوران درد دارای گیرنده های مواد افیونی هستند که در آنها مواد افیونی اگزوژن و درون زا می توانند توانایی انتقال اطلاعات درد را تعدیل کنند. علاوه بر این، تراکم بالایی از گیرنده های مواد افیونی در خاکستری اطراف قناتی، یا PAG، هسته رافه مگنوس، یا NRM، و رافه پشتی، یا DR، از بصل النخاع شکمی، در نخاع، هسته دمی، یا CN، هسته سپتوم یافت می شود. هیپوتالاموس، هابنولا و هیپوکامپ. اپیوئیدهای تجویز شده به صورت سیستمی در دوزهای ضد درد، مکانیسم های نخاعی و فوق نخاعی را از طریق ?،?، و? گیرنده های اپیوئیدی را تایپ کنید و سیگنال های درد را برای تعدیل علائم تنظیم کنید.
مدارهای عصبی و مدولاسیون درد
برای چندین دهه پیشنهاد شده است که در جایی در سیستم عصبی مرکزی یک مدار وجود دارد که می تواند جزئیات درد ورودی را مدوله کند. نظریه کنترل دروازه و سیستم انتقال صعودی / نزولی دو پیشنهاد از چنین مدار است. در زیر، ما هر دو را در جزئیات بیشتر بحث خواهیم کرد.
نظارت بر دروازه
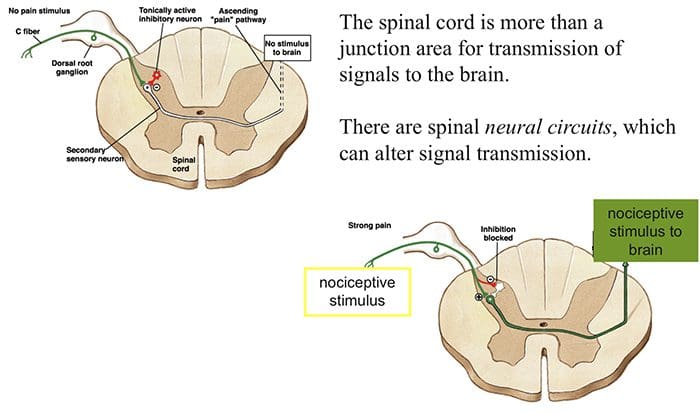
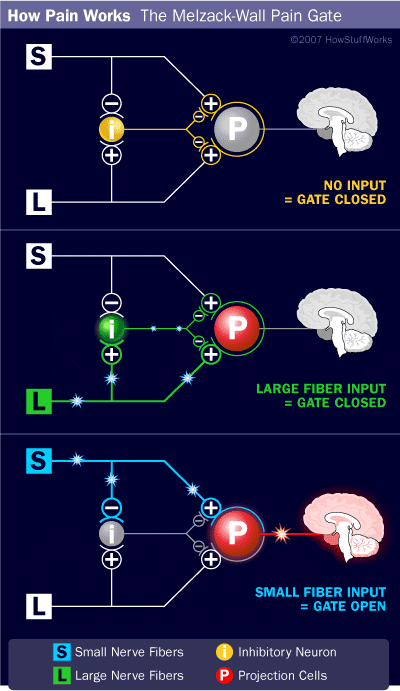
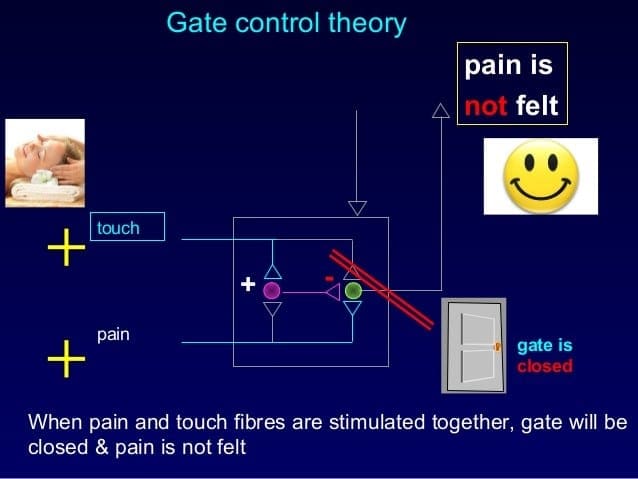
مکانیسم مدولاتور درد شناخته شده به عنوان نظریه کنترل دروازه، توسط Melzack و وال در اواسط 1960 پیشنهاد شده است. مفهوم نظریه کنترل دروازه این است که ورودی غير دردناک دروازه ها را به ورودی دردناک بسته می کند، که منجر به اجتناب از احساس درد از سفر به CNS می شود، به عنوان مثال، ورودی های غیر خطرناک یا تحریک، سرکوب درد است.
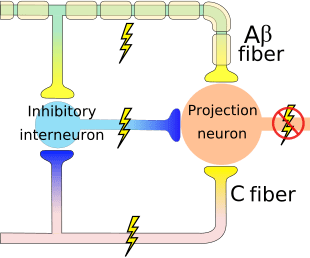
این نظریه نشان می دهد که collaterals از الیاف حساس بزرگ حمل ورودی حسی پوستی فعال interneurons مهار، که مهار و تنظیم داده های انتقال درد از الیاف درد است. ورودی های غیر خطرناک مهار درد، ورودی حسی و دروازه را به ورودی های مضر بسته می کند. نظریه کنترل دروازه نشان می دهد که در سطح نخاعی، تحریک غیرخوابی باعث جلوگیری از پیشگیری از پوکی استخوان در ریشه های عصبی ریشه می شود که سیناپس بر روی نورون های ستون فقرات عضلانی (T) است. این مهار پیشگیری از جلوگیری از ورود اطلاعات بدخواهانه از دسترسی به CNS جلوگیری می کند، مثلا دروازه به اطلاعات سمی ورودی بسته می شود.
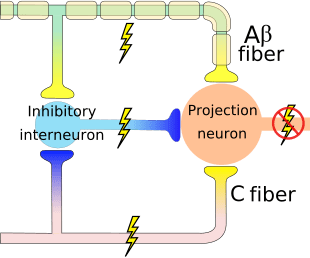
نظریه کنترل دروازه، منطق ایده ای برای تولید و استفاده از تحریک عصبی الکتریکی پوستی یا TENS، برای تسکین درد بود. به منظور موثر بودن، واحد TENS دو فرکانس کنونی مختلف را در زیر آستانه درد ایجاد می کند که می تواند توسط بیمار گرفته شود. این فرایند درجه پیشرفت در درمان درد مزمن را پیدا کرده است.
مدولاسیون درد: نظریه کنترل دروازه
تحریک تولید ناخالصی (SPA)
شواهدی برای یک سیستم آنژگی ذاتی توسط تحریک الکتریکی داخل جمجمه ای از مناطق مغز گسسته مشخص شده است. این مناطق به همراه هسته های دیگر، خاکستری پرآبی، یا PAG و هسته رافا مگنوس، یا NRM، ریف پشتی یا DR، هسته کادات یا CN، هسته سپتوم یا Spt هستند. چنین تحریک یا سیگنال های حسی، مهار درد، ایجاد درد زایمان بدون سرکوب رفتاری، در حالی که احساس لمس، درجه حرارت و فشار به طور کامل باقی می ماند. با توجه به مطالعات انجام شده، اسپاسم یا تحریک ناخوشایند تولید شده، واضح تر است و برای دوره طولانی تر بعد از تحریک در انسان همچنان در حیوانات آزمایش می شود. علاوه بر این، در طول SPA، افراد، با این حال، هنوز هم به تحریک غیرخون مانند درجه حرارت و لمس در منطقه محدود ناشتا واکنش نشان می دهند. موثرترین CNS ها یا مناطق سیستم عصبی مرکزی برای ایجاد SPA، در PAG و هسته راف یا RN قرار می گیرند.
تحریک الکتریکی از PAG یا NRM از سلول های تالامال نخاعی یا نورون های نخاعی که در لامینا I، II و V به صورت تک نفس به مغز تزریق می کنند، مهار می شود تا اطمینان حاصل شود اطلاعات مضر از ناسسیپتورها که در نهایت در سطح نخاعی مدوله می شوند. علاوه بر این، PAG دارای اتصالات عصبی به هسته rafe magnus یا NRM است.
فعالیت PAG به احتمال زیاد بوسیله فعال سازی مسیر نزولی NRM و احتمالا همچنین با فعال شدن اتصالات صعودی بر روی سطوح زیرکوریتی بیشتر CNS رخ می دهد. علاوه بر این، تحریک الکتریکی PAG یا NRM موجب برانگیختگی رفتاری و یا تحریک ناخوشایند می شود. تحریک ایجاد analgesia، و یا SPA باعث آزاد شدن اندورفین ها می شود که توسط نالوکسون آنتاگونیست اپیدمی مسدود می شود.
در طول تحریک PAG و یا RN، سروتونین، همچنین به صورت پزشکی به عنوان 5-HT شناخته می شود، همچنین می تواند از آکسون صعودی و نزولی از هسته های زیرکوریته، در هسته های تریدمینال نخاعی و در نخاع تخلیه شود. این نسخه از 5-HT، مانع یا مسدود کردن عصب ورودی می شود و انتقال درد را تنظیم می کند. از بین بردن 5-HT با ضایعات الکتریکی هسته ریفه یا با یک ضایعه عصبی عصبی که به وسیله تزریق موضعی یک عامل شیمیایی مانند پاراكلروفرنیلالانین یا PCPA ساخته شده است، منجر به مسدود كردن قدرت opiate می شود، چه در داخل جمعی و چه سیستمی، تحریک الکتریکی به منظور تولید درد بیهوشی.
برای تأیید اینکه اگر تحریک الکتریکی با استفاده از انتشار اپید و دوپامین، درد ناشی از درد را ایجاد کند، منطقه به صورت مورفین یا 5-HT به صورت میکروتیک تزریق می شود. تمام این میکروزیابی ها در نهایت باعث درد زا می شود. این فرآیندها همچنین راهی برای شناسایی مناطق مغزی مرتبط با سرکوب درد فراهم می کنند و به ایجاد یک نقشه مرکز درد کمک می کنند. موثرترین روش تولید آنتیبیوتیک مخدر، یا OA، تزریق داخل مغزی مرفین به PAG است.
PAG و RN و همچنین سایر ساختارهای مغز که در آن تولید بیهوشی تولید می شود نیز دارای گیرنده های اپیداییک هستند. تجویز مواد مخدر در داخل مغز باعث ایجاد درد شدید و اسپاسم می شود، به وسیله سیستمیک یا از میکروکنترل داخلی نالوکسون، آنتاگونیست مرفین، به PAG یا RN. به همین دلیل، پیشنهاد شده است که دو، هر دو OA و SPA، توسط مکانیزم مکرر عمل می کنند.
اگر OA و SPA از طريق يك سيستم ذاتي رفتار كنند، پس فرضي كه opiates فعاليت مكانيزم كنترل درد را بسيار بيشتر مي كند. در حقيقت، شواهد موجود نشان ميدهند که ريزنشتهايي از مواد مخدر در PAG، يک سيستم مغز استخواني را فعال ميکند که مانع انتقال درد در سطوح نخاعي گردن ميشود. این مشاهدات به این معنی است که ضد درد ناشی از خاکستری پرآبی، یا PAG، نیازمند مسیر نزولی به نخاع است.

دکتر الکس جیمنز Insight
مدولاسيون درد از طريق فرآيند تحريک مغناطيسي الکتريکي رخ مي دهد که به علت فعال شدن فيبرهاي مهار کننده نزولي که باعث تنظيم يا مهار ورودي و خروجي نورون هاي خاص مي شود، رخ مي دهد. اعتقاد بر این که آنچه که آنتاگونیست های اپیدمی و سروتونرژیک توصیف شده است، هر دو موضع ضد درد موضعی و محرک های مغز ایجاد می کنند. سیگنال های حسی یا امواج در سیستم عصبی مرکزی در نهایت توسط سیستم های مهار کننده صعودی و نزولی تحت کنترل قرار می گیرند، از مواد مخدر اندوژن یا سایر مواد درونی مانند سروتونین به عنوان واسطه های مهار کننده استفاده می شود. درد درک پیچیده ای است که می تواند تحت تاثیر عوامل مختلفی از جمله حالت احساسی قرار گیرد.
مکانیسم های مدولاسیون درد
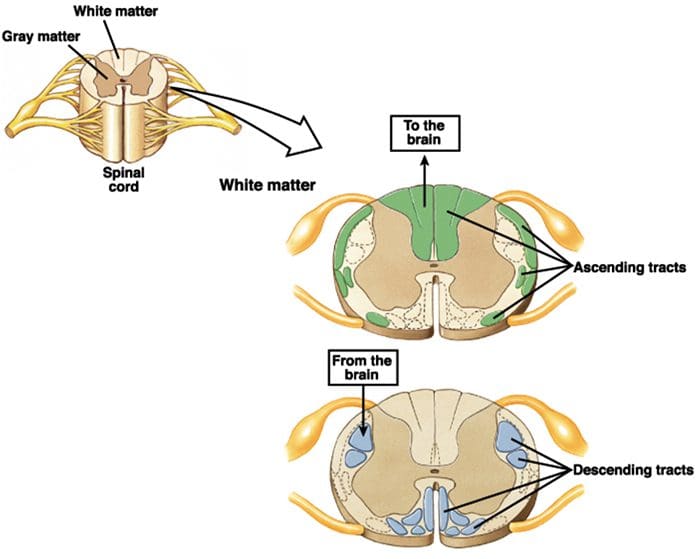
مکانیسم سرکوب صعودی و نزولی
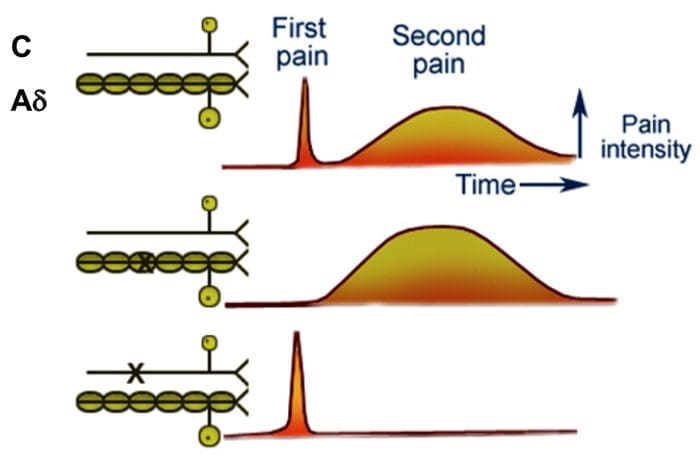
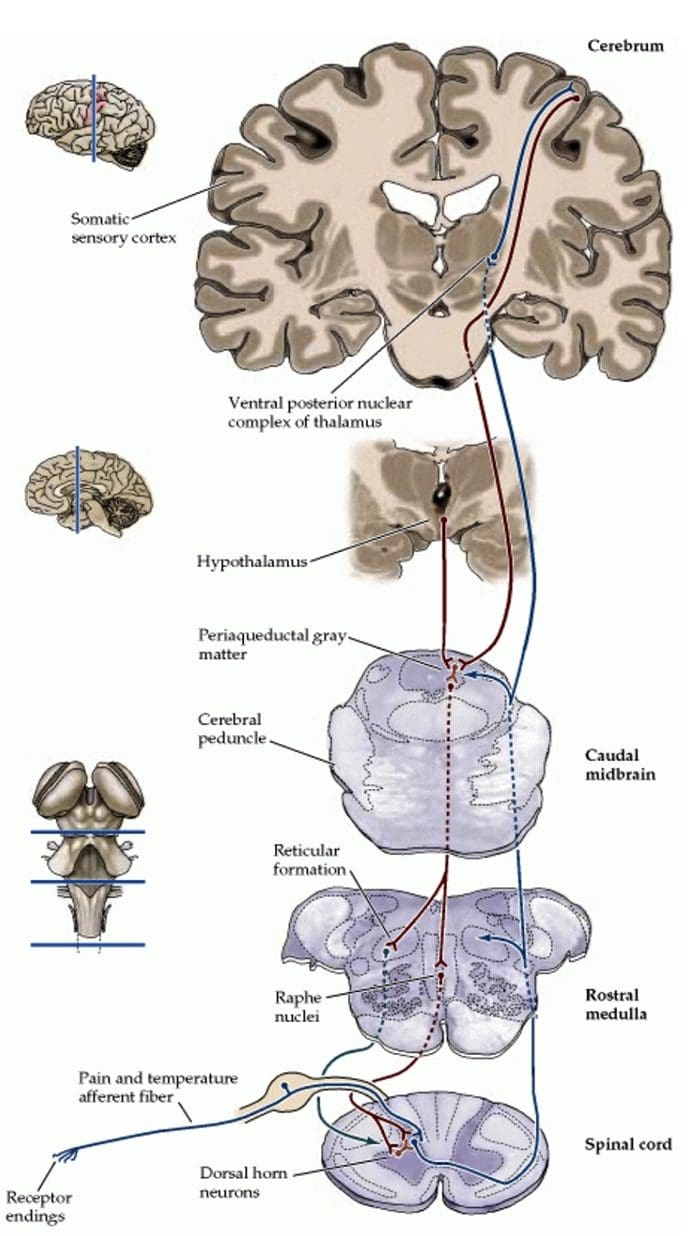
فیبرهای درد اولیه صعودی، مانند A ? و فیبرهای C، از نواحی عصبی محیطی به شاخ پشتی نخاع می رسند تا نورون های گیرنده درد را در Rexed laminae I & II عصب دهی کنند. سلول های Rexed lamina II اتصالات سیناپسی را در لایه های Rexed IV تا VII ایجاد می کنند. سلولها، بهویژه در لایههای I و VII شاخ پشتی، باعث ایجاد مجاری اسپینوتالاموس صعودی میشوند. در سطح ستون فقرات، گیرنده های مواد افیونی در انتهای پیش سیناپسی نورون های عصبی خود و در لایه های سطح بین عصبی IV تا VII از شاخ پشتی قرار دارند.
فعالسازی گیرندههای مواد افیونی در سطح بینعصبی، هیپرپولاریزاسیون نورونها را تولید میکند که منجر به مهار فعالسازی و همچنین آزاد شدن ماده P، یک انتقالدهنده عصبی دخیل در انتقال درد میشود، بنابراین از انتقال درد جلوگیری میکند. مداری که از ماده خاکستری اطراف قناتی یا PAG در بالای ساقه مغز، لوکوس سرولئوس یا LC، هسته رافه مگنوس یا NRM و هسته رتیکولاریس gigantocellularis یا Rgc تشکیل شده است، منجر به درد نزولی می شود. مسیر سرکوب، که دادههای دریافتی درد را در سطح نخاع مهار میکند.
همانطور که قبلا ذکر شد، opioids با گیرنده های مخدر در سیستم های متمایز سیستم عصبی مرکزی ارتباط برقرار می کنند. این گیرنده های مخدر منطقه ای طبیعی برای هورمون ها و مواد مخدر اندوژن مانند آندورفین ها و انکافیلین ها هستند. با توجه به اتصال در گیرنده در وب سایت های زیرکوریتی، تغییرات ثانویه ای که منجر به تغییر در خواص الکتروفیزیولوژیکی نورون ها و تنظیم اطلاعات درد صعودی می شوند.
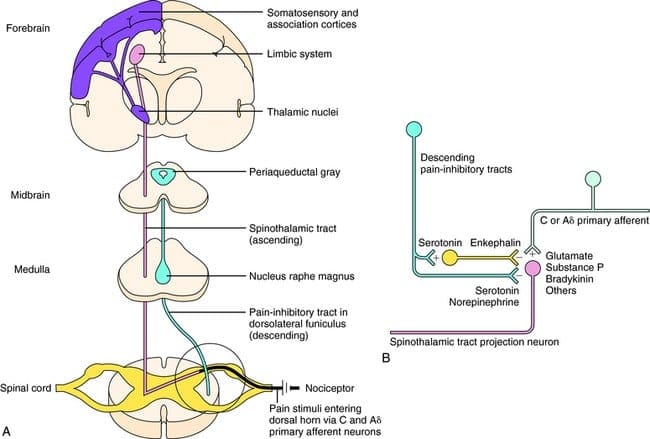
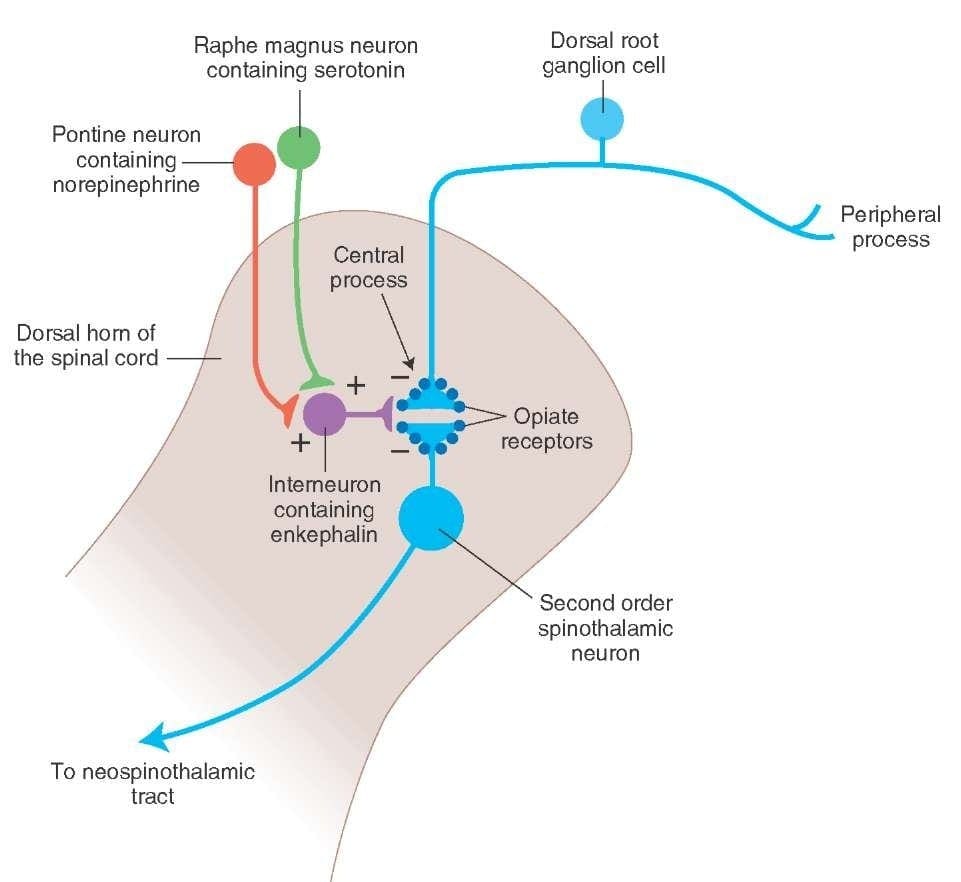
چه چیزی PAG را فعال می کند تا عواقب آن را اعمال کند؟ کشف شد که تحریک زهرآگین باعث ایجاد نورون در هسته reticularis gigantocellularis یا RGC می شود. هسته Rgc هر دو PAG و NRM را جذب می کند. PAG آکسون را به NRM می فرستد و اعصاب در NRM آکسون ها را به طناب نخاعی می فرستد. علاوه بر این، ضایعات دو طرفه دو طرفه یا DLF، که به عنوان DLFX نامیده می شوند، مسکن ضد درد تولید شده توسط هر دو تحریک الکتریکی و تزریق مستقیم مواد مخدر را به طور مستقیم به PAG و NRM مسدود می کنند، اما آنها فقط باعث کاهش اثرات ضد درد موضعی opiates می شوند. این مشاهدات از فرضیه حمایت می کند که مسیرهای نزولی گسسته از DLF برای OA و SPA مورد نیاز است.
DLF شامل فیبر هایی است که از چند هسته مغز هسته ای تشکیل شده اند که می توانند از طریق عصب های داخل هسته rafe magnus یا NRM سروتونرژیک باشند یا 5-HT؛ نورونهای دوپامینرژیکی ناشی از ناحیه تنگنال شکمی، یا VTA، و نورونهای آدرنرژیک ناشی از لوکوس کورولوس یا LC. این فیبرهای نزولی باعث می شود ورودی های خطرناک در نورون های نخاعی نوکسیپتوم در لامینا I، II، و V.
گیرنده های Opiate نیز در شاخ پشتی نخاع کشف شده است، به ویژه در Rexed laminae I، II، و V، و گیرنده های اپیدمی چنین افرادی را می توانند تأثیر مهمی بر روی نورون های شاخۀ عقب و انتقال اطلاعات ناسازگارانه داشته باشند. به نظر می رسد اثر مورفین به طور مساوی در هسته نخاعی و هسته مغز، از جمله PAG و NRM به طور مساوی اعمال می شود. سیستمیک مورفین بر روی هر دو از گیرنده های اپیدمی نخاعی مغز و مغز عمل می کند تا باعث ایجاد درد شدید شود. مورفین گیرنده های اپیدمی مغز استخوان را به وجود می آورد که باعث می شود مسیر سرتونی اورژانسی نزولی در مغز به داخل نخاع و همچنین DLF منجر شود و این سیناپس به وسیله مواد مخدر در سطح نخاعی قرار دارد.
این مشاهدات نشان می دهد که محرک های خطرناک، به جای محرک های غیر قابل هضم، نظریه کنترل دروازه را تعیین می کنند که برای فعال شدن مدولاسیون مداخله درد ناکافی است که درد از طریق مسیر نزولی DLF مهار می شود. علاوه بر این، اتصالات صعودی در PAG و هسته رافه به مجموعه PF-CM وجود دارد. این مناطق تالامیک بخشی از مدولاسیون درد صعودی در درجه دیویدسفالون است.
فشارخون ناشی از استرس (SIA)
ممکن است ناخوشایند ممکن است در شرایط خاصی ایجاد شود. قرار گرفتن در معرض بسیاری از وقایع تنش زا یا دردناک، پاسخ زخم را ایجاد می کند. این پدیده به عنوان استرس ناشی از کم خونی شناخته شده است، یا SIA. اعتقاد بر این است که تحریک ناشی از استرس موجب بروز فاکتورهای فیزیولوژیک و روانشناختی می شود که باعث کنترل درد درونی و سیستم های اپیدمی می شود. به طور مثال، سربازانی که در جنگ زخمی شده اند و یا ورزش هایی که در ورزش آسیب دیده اند گاهی اوقات گزارش می دهند که در طول نبرد یا بازی احساس درد و یا ناراحتی نمی کنند، با این وجود، پس از آنکه وضعیت خاصی متوقف شد، درد از بین می رود. در حیوانات نشان داده شده است که شوک الکتریکی موجب بی اشتهایی ناشی از استرس می شود. بر اساس این آزمایشات، فرض شده است که فشار سربازان و ورزشکاران تجربه درد را که بعدا تجربه می کنند، سرکوب می کند.
اعتقاد بر این است که مواد مخدر غنی در واکنش به استرس و مهار درد توسط راه اندازی سیستم نزولی میانه ای تولید می شود. علاوه بر این، برخی از SIA ها با استفاده از آنتیبیوتیک مخدر تحمل متقابل نشان دادند که نشان دهنده این است که این اسپیگرافی از طریق گیرنده های اپیدمی تأمین می شود. آزمایشات با استفاده از پارامترهای مختلف تحریک شوک الکتریکی نشان می دهد که آنژیوگرافی ناشی از استرس و برخی از این اضطراب هایی که باعث ایجاد درد شدید می شود توسط نالوكسان آنتاگونیست مهاركننده مسدود می شود، در حالی كه دیگران توسط نالوكسان مسدود نمی شوند. در نتیجه، این مشاهدات منجر به تصمیم گیری می شود که هر دو از فرم های مخدر و غیر مخدر SIA وجود دارد.
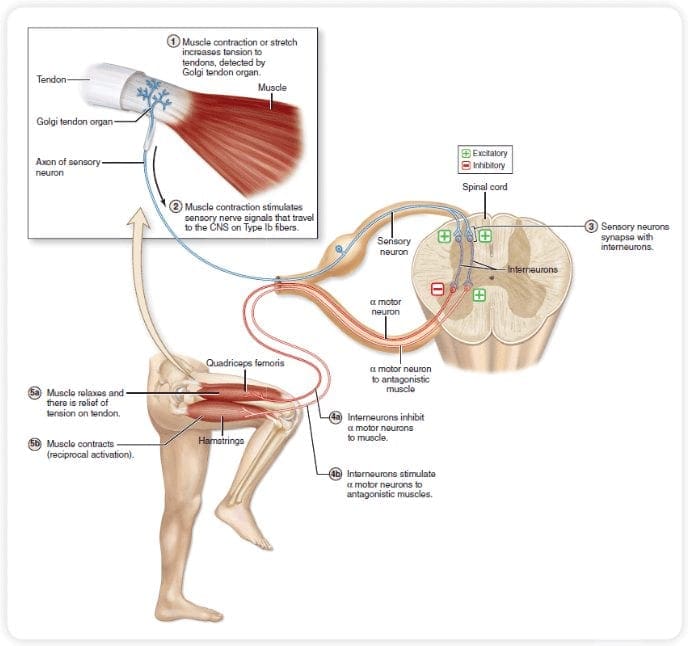
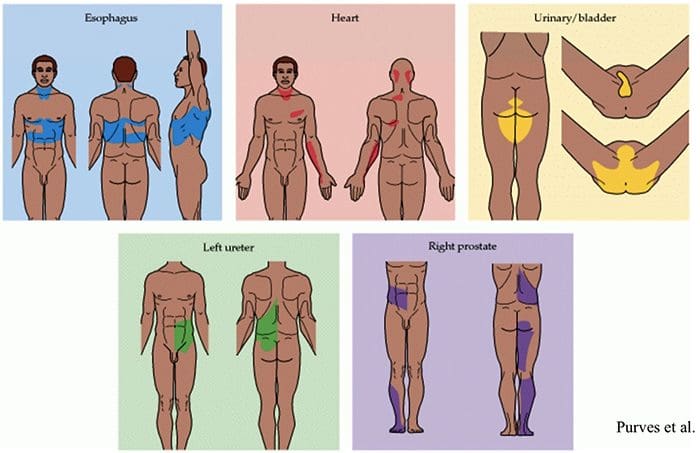
رفلکس سوماتوسیس
رفلکس somatovisceral یک رفلکس است که در آن تومورهای احشایی فعال یا مهار شده توسط تحریک حساسیت جسمی. در حیوانات آزمایشی، هر دو تحریک مضر و بی خطر از عصب های فیزیوتراپی اثبات می کنند که تغییرات رفلکس در فعالیت مؤثر سمپاتیک، و در نتیجه، عملکرد عضو ارجح است. این پدیده ها در مناطقی مانند دستگاه گوارش، دستگاه ادراری، مدول آدرنال، سلول های لنفاوی، قلب و عروق مغز و اعصاب محیطی نشان داده شده است.
اغلب، برشها به صورت تجربی با تحریک پوستی پوستی ایجاد می شود، حتی اگر برخی از کارها بر روی عضلات و مفصل مفصلی، از جمله سلول های ستون فقرات انجام شده است. واکنش های نهایی نشان دهنده ادغام چندین اثر تونیک و رفلکس است و ممکن است گرایش های جانبی و رگلاتال و همچنین تحریک پذیری متغیر را با خطراتی که دارد در بر داشته باشد. با توجه به پیچیدگی و چندگانگی مکانیسم هایی که در آخرین بیان واکنش رفلکس درگیر شده اند، تلاش برای به کارگیری شرایط بالینی به احتمال زیاد باید به نفع مطالعات فیزیکی بیشتر سیستماتیک انجام شود.
محدوده اطلاعات ما محدود به کیهان شناسی و همچنین آسیب های ناشی از ستون فقرات و شرایط است. برای بحث در مورد موضوع، لطفا از دکتر جیمنز بپرسید یا با ما تماس بگیرید 915-850-0900 .
دکتر الکس جیمنز سرپرستی می کند
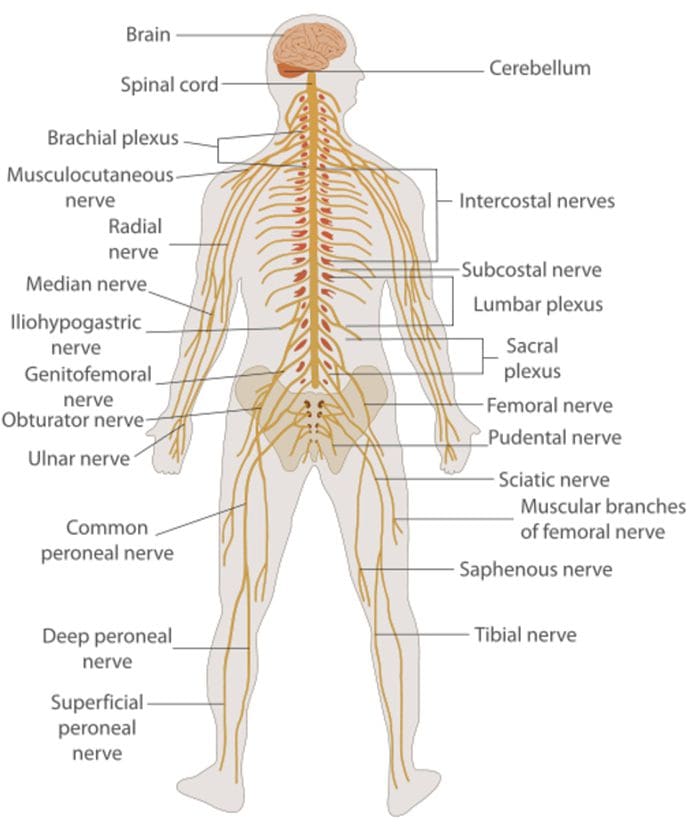
موارد اضافی: سیاتیک
سیاتیک از نظر پزشکی به عنوان مجموعه ای از علائم شناخته شده است، نه یک آسیب و / یا یک وضعیت واحد. علائم درد عصب سیاتیک یا سیاتیک می تواند با شدت و فرکانس متفاوت باشد، اما اغلب به عنوان ناگهانی، چاقو یا درد الکتریکی توصیف می شود که از پایین کمر عقب پایین باسن، باسن، ران و پاها را به پای سایر علائم سیاتیک ممکن است شامل احساس سوزن شدن یا سوزش، بی حسی و ضعف در طول طول عصب سیاتیک باشد. سیاتیک اغلب افراد سالهای 30 و 50 را تحت تاثیر قرار می دهد. این ممکن است اغلب به علت انحطاط ستون فقرات به علت سن ایجاد شود، اما فشرده سازی و تحریک عصب سیاتیک ناشی از انفجار یا دیسک حنجره، در میان سایر مسائل مربوط به سلامت ستون فقرات، همچنین ممکن است درد عصب سیاتیک ایجاد کند.

موضوع فوق العاده مهم: علائم Chiropractor سیاتیک



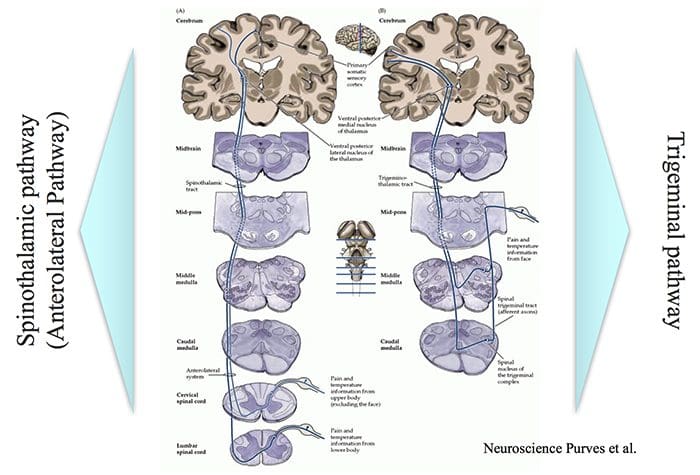
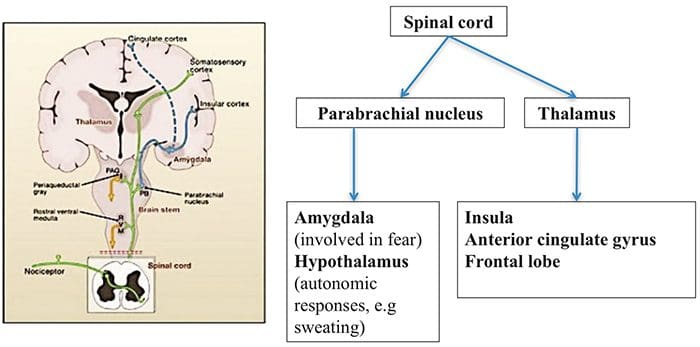 نواحی مغز درگیر در پردازش سیگنال های درد
نواحی مغز درگیر در پردازش سیگنال های درد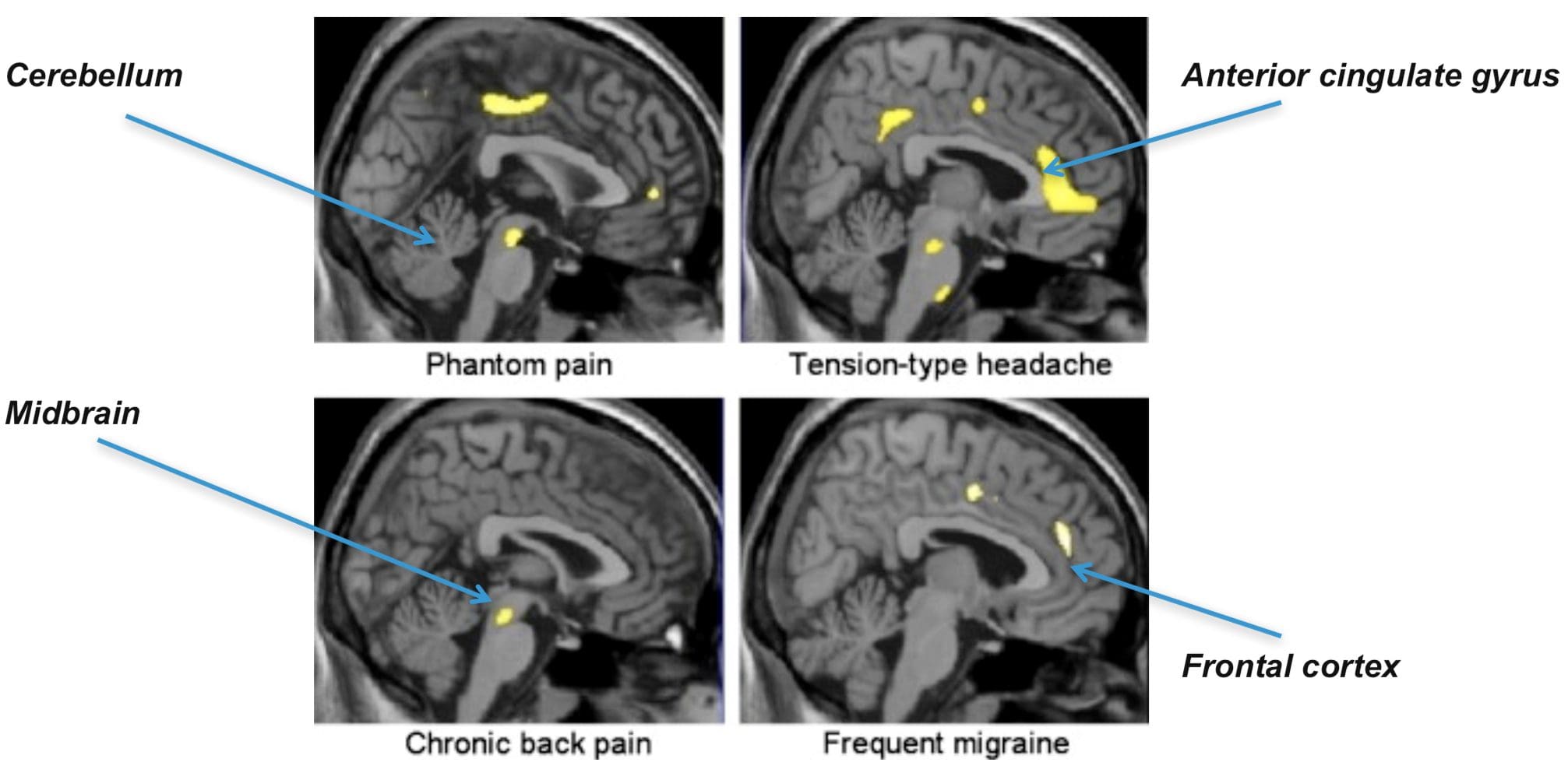 سینگولات قدامی و قشر اینسولا در افراد انسانی فعال می شوند
سینگولات قدامی و قشر اینسولا در افراد انسانی فعال می شوند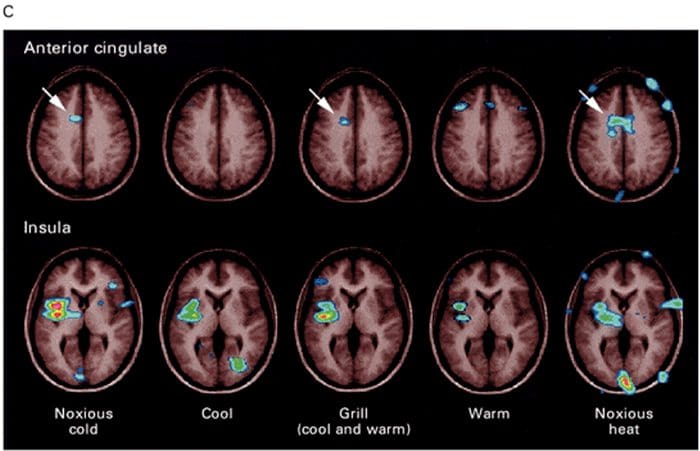
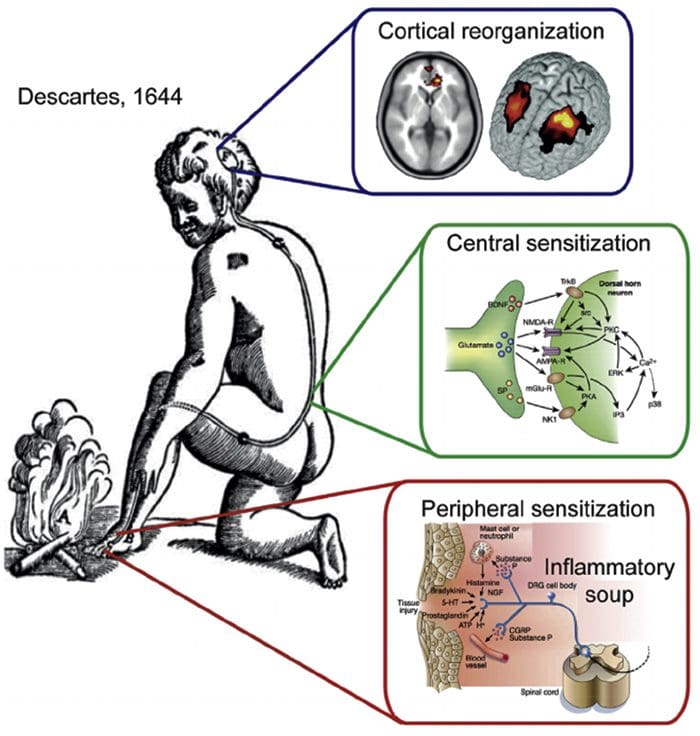
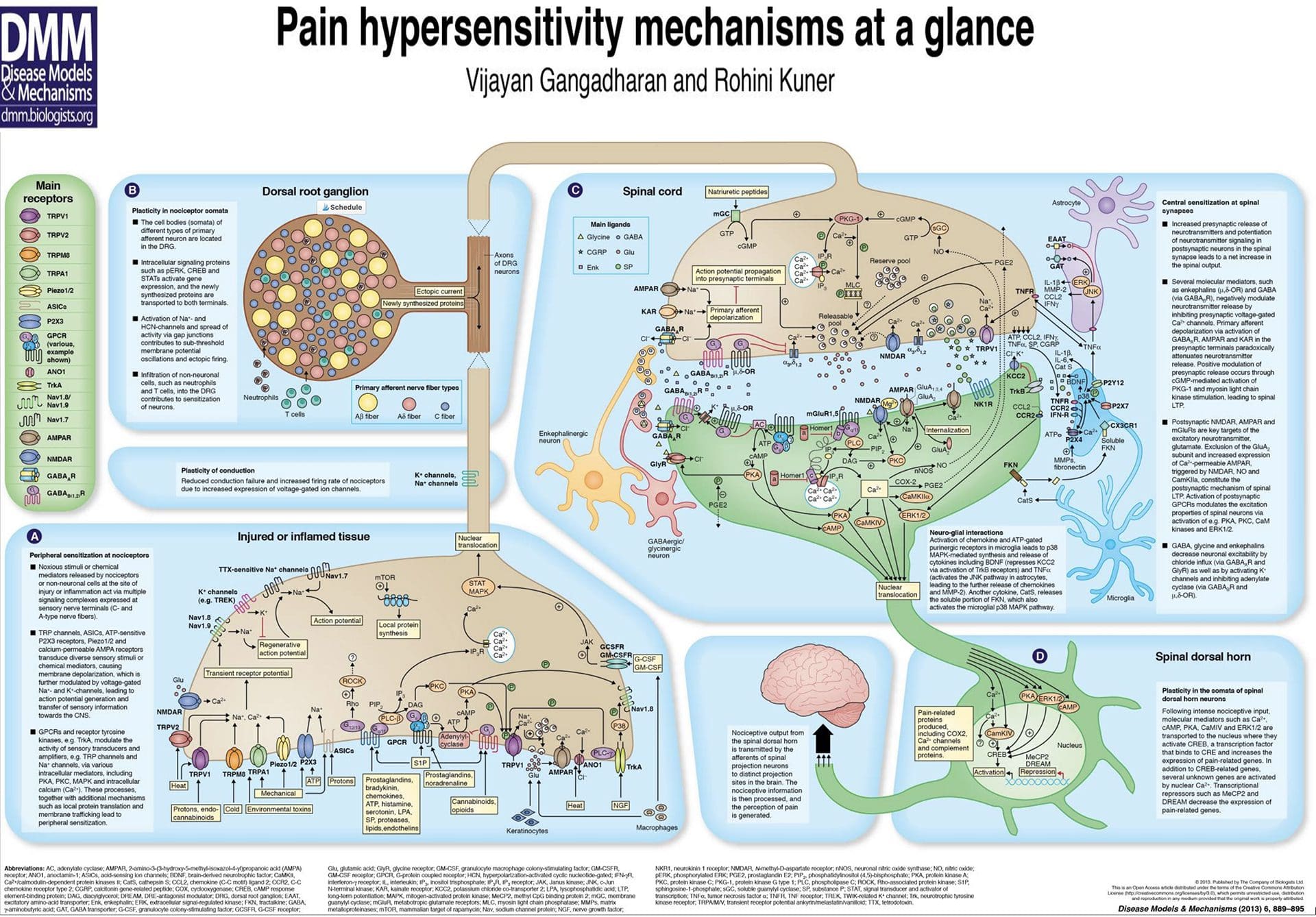
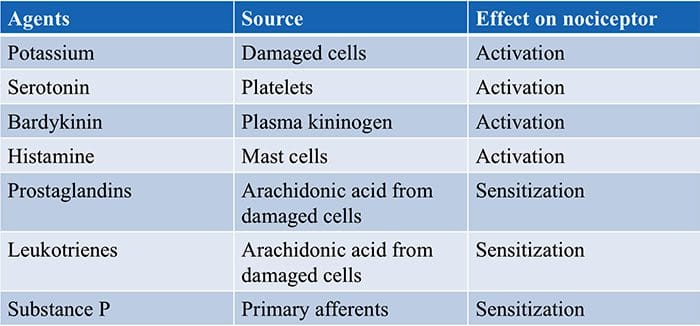
 سوپ التهابی - پردردی
سوپ التهابی - پردردی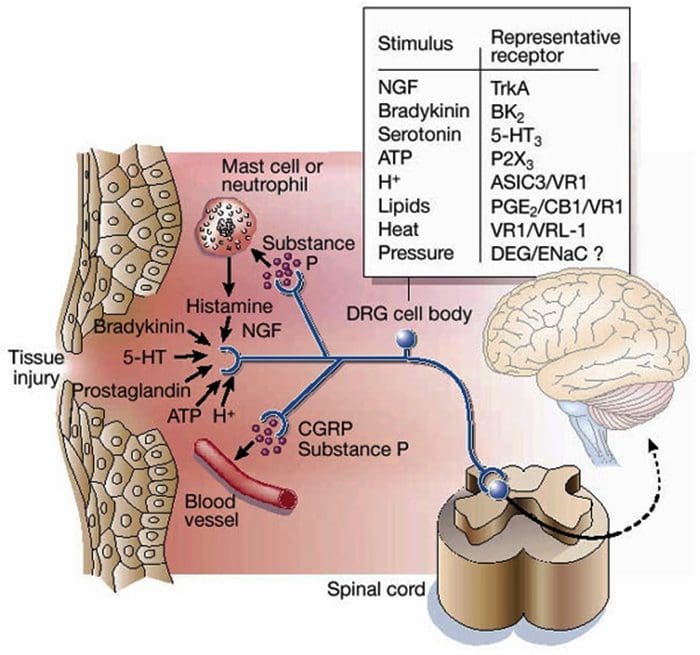
 تئوری کنترل دروازه درد
تئوری کنترل دروازه درد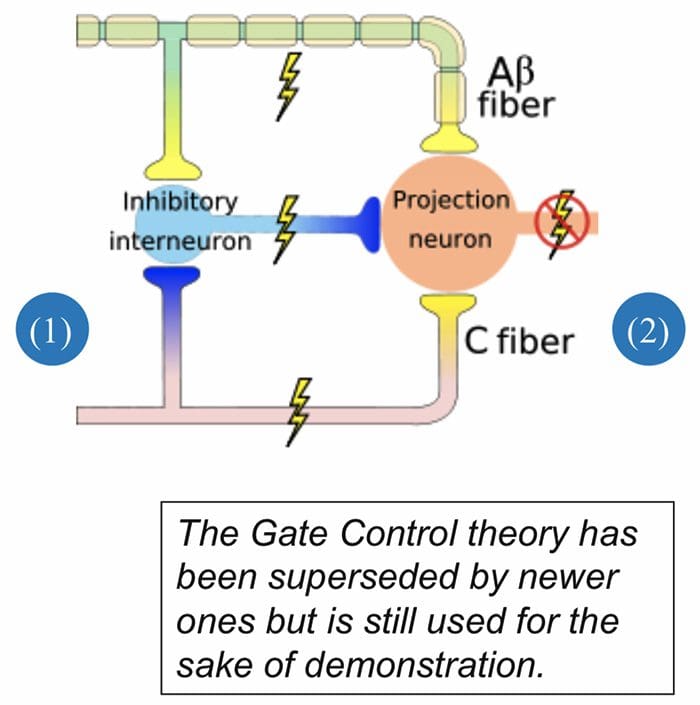
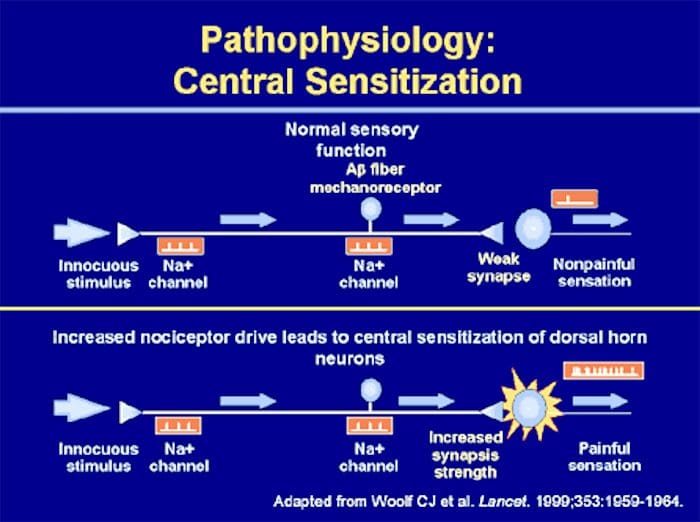
 ناهنجاری های سیستم درد
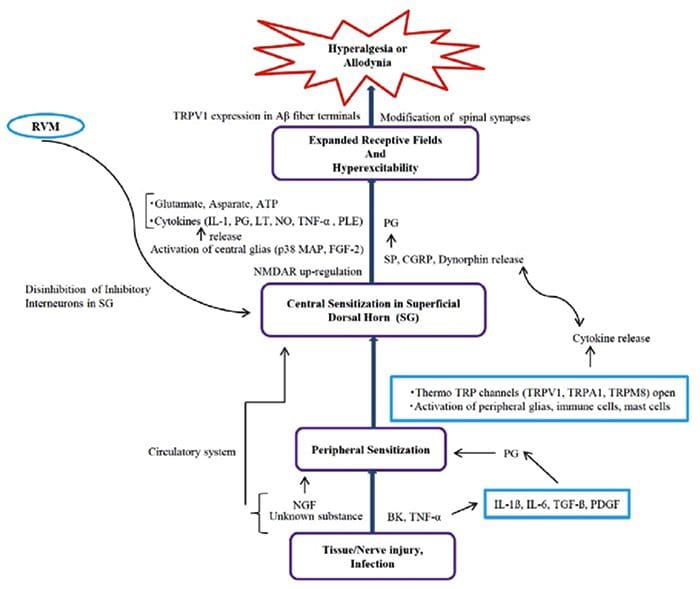
ناهنجاری های سیستم درد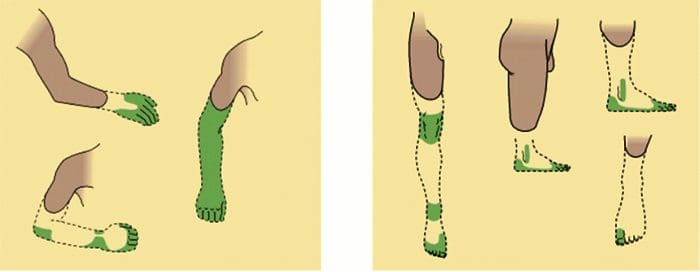 حساسیت محیطی
حساسیت محیطی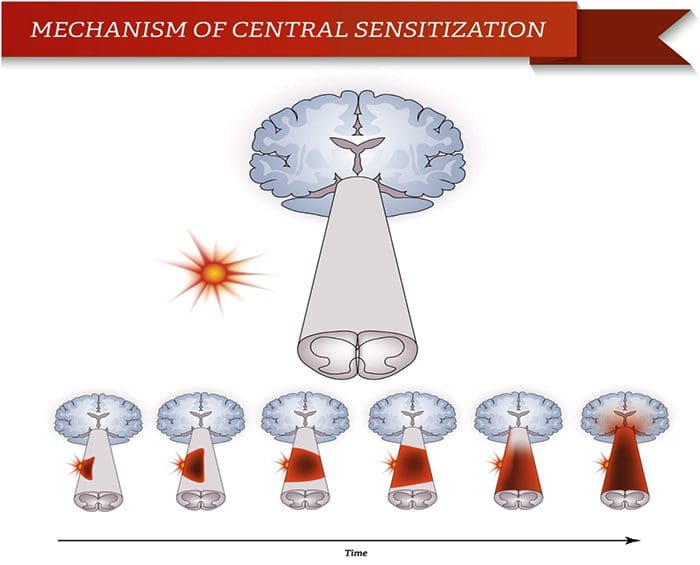
 سازمان قشر حسی تنی
سازمان قشر حسی تنی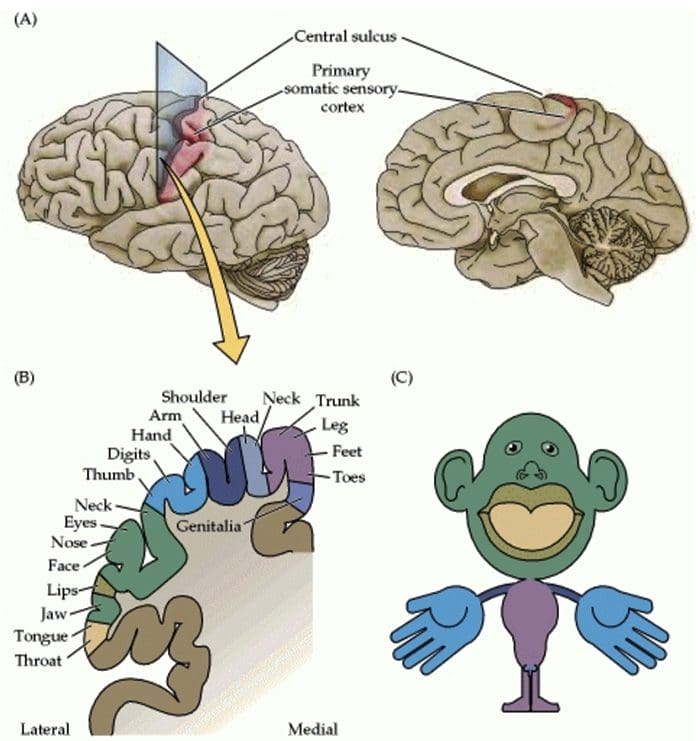 سازماندهی مجدد قشر مغز
سازماندهی مجدد قشر مغز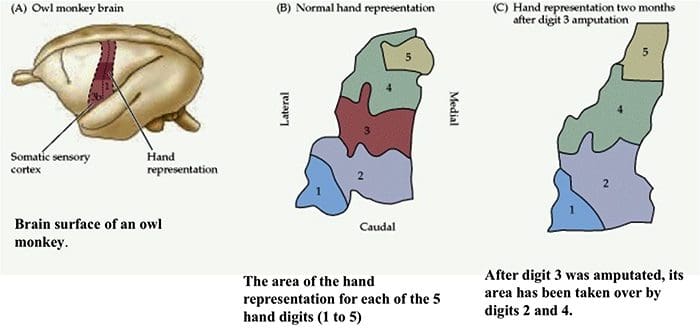

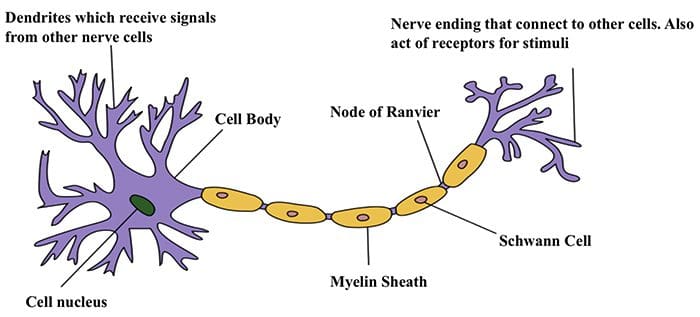 ارتباط سلول عصبی با سلول عصبی
ارتباط سلول عصبی با سلول عصبی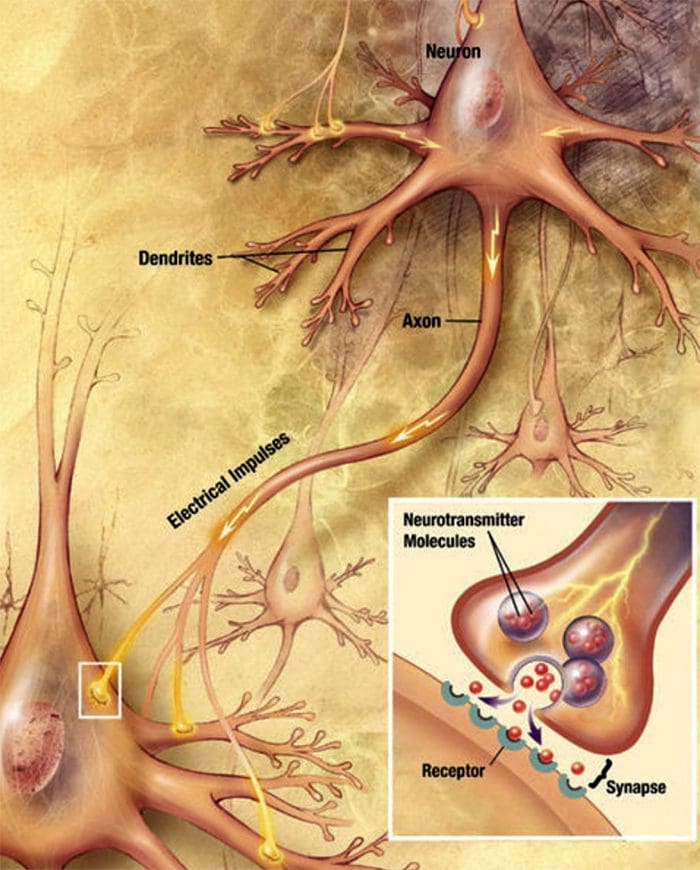 سلول های عصبی با آزاد کردن یک ماده شیمیایی از انتهای عصبی با سلول های دیگر ارتباط برقرار می کنند. انتقال دهنده های عصبی
سلول های عصبی با آزاد کردن یک ماده شیمیایی از انتهای عصبی با سلول های دیگر ارتباط برقرار می کنند. انتقال دهنده های عصبی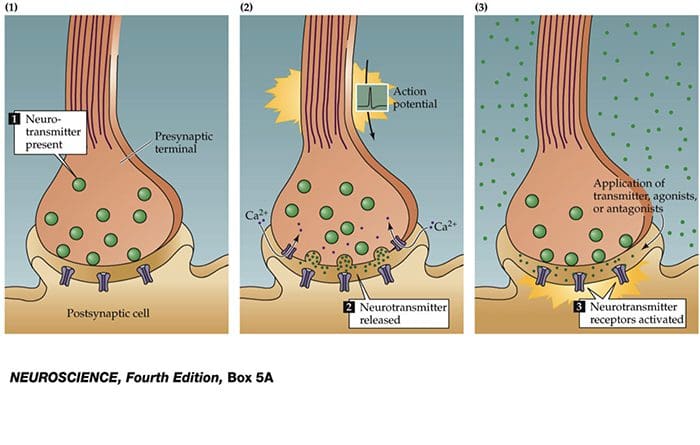
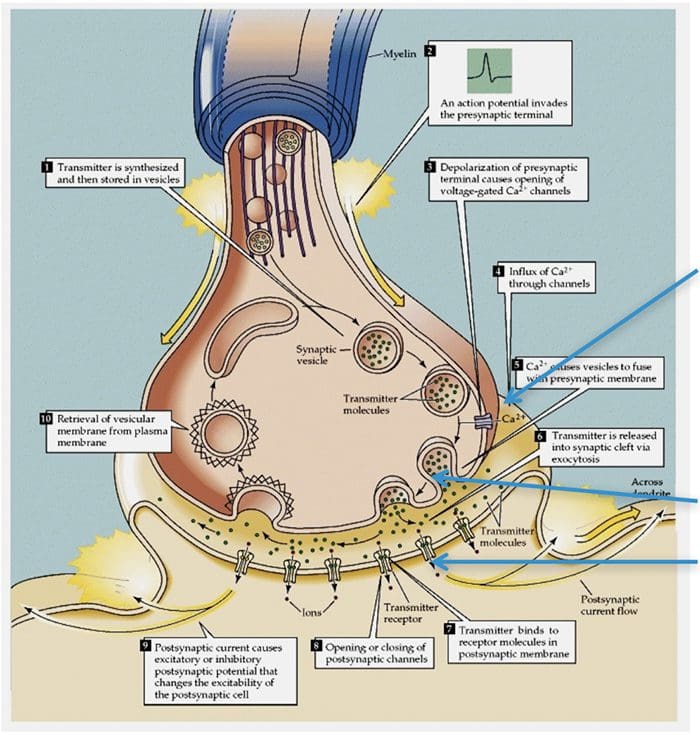
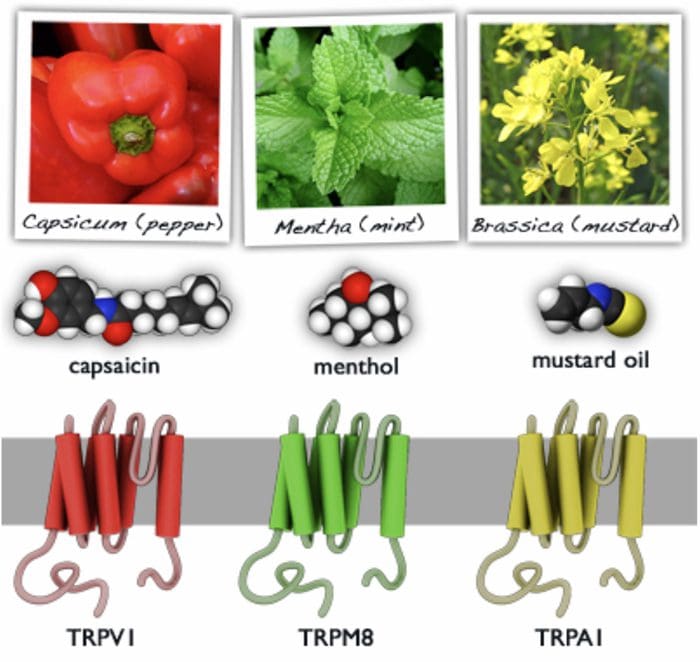
 کانال های TRP
کانال های TRP