فهرست
درک رژیم تقلید روزه ProLon
روزهداری با مزایای سلامتی فراوانی همراه است از از دست دادن وزن تا طول عمر. انواع مختلفی از روش های روزهداری مانند روزهداری متناوب وجود دارد. رژیم غذایی روزمره اجازه می دهد تا شما از مزایای روزه داری سنتی بدون محرومیت از مواد غذایی خود بهره مند شوید. تفاوت اصلی FMD این است که به جای اینکه تمام غذاها را به طور کامل برای چندین یا حتی چند هفته از بین ببرد، شما تنها مصرف کالری خود را برای مدت پنج روز از ماه محدود می کنید.
در حالیکه هر کسی می تواند خود را به طور طبیعی تحت کنترل بگیرد ProLon رژیم غذایی روزمره برنامه غذایی غذایی روزانه 5 ارائه می دهد که هر روز به صورت جداگانه بسته بندی و برچسب گذاری می شود و غذاهای مورد نیاز شما را برای میزان FMD در مقادیر و ترکیبات دقیق در اختیار شما قرار می دهد. برنامه غذا از غذاهایی آماده به غذا یا آسان آماده تهیه می شود، از جمله میله ها، سوپ ها، تنقلات، مکمل ها، کنسانتره نوشیدنی و چای ها. محصولات علمی فرموله شده و مزه عالی هستند. قبل از شروع رژیم تقلید روزه ProLon ، برنامه 5 روزه وعده غذایی، لطفا مطمئن شوید که با یک متخصص مراقبت های بهداشتی تماس بگیرید تا متوجه شوید که آیا FMD برای شما مناسب است یا خیر. هدف از پژوهش حاضر، نشان دادن مکانیزم های مولکولی و کاربرد بالینی ناشتا در سکته قلبی است.
روزه گیری: مکانیسم های مولکولی و برنامه های بالینی
روزه برای هزاره ها تمرین شده است، اما تنها
معرفی
در انسان ها ، روزه گرفتن با خوردن هیچ یا حداقل مقدار مواد غذایی و نوشیدنی های کالری برای دوره هایی که به طور معمول از 12 ساعت تا سه هفته است ، حاصل می شود. بسیاری از گروه های مذهبی دوره های روزه داری را در آداب و رسوم خود گنجانند از جمله مسلمانانی که از طلوع فجر تا غروب ماه رمضان روزه می گیرند و مسیحیان ، یهودیان ، بودایی ها و هندوها که به طور سنتی در روزهای تعیین شده هفته یا سال تقویمی روزه می گیرند. در بسیاری از کلینیک ها ، بیماران در حال گذراندن دوره های ناشتا فقط با آب یا بسیار کم کالری (کمتر از 200 کیلوکالری در روز) ناشتا با مدت زمان 1 هفته یا بیشتر برای کنترل وزن و پیشگیری و درمان بیماری ، توسط پزشکان تحت نظر قرار می گیرند. روزه داری از محدودیت کالری (CR) متمایز است که در آن میزان کالری دریافتی روزانه به میزان 20-40٪ کاهش می یابد ، اما دفعات وعده غذایی حفظ می شود. گرسنگی در عوض یک نارسایی تغذیه ای مزمن است که معمولاً به عنوان جایگزین کلمه روزه داری به ویژه در یوکاریوت های تحتانی استفاده می شود ، اما همچنین برای تعریف انواع شدید روزه داری که می تواند منجر به انحطاط و مرگ شود ، استفاده می شود. اکنون می دانیم که روزه داری منجر به کتوژنیز می شود ، باعث ایجاد تغییراتی در مسیرهای متابولیکی و فرآیندهای سلولی مانند مقاومت در برابر استرس ، لیپولیز و اتوفاژی می شود و می تواند دارای کاربردهای پزشکی باشد که در بعضی موارد به اندازه داروهای تایید شده مانند کاهش تشنج موثر است. و آسیب مغزی مرتبط با تشنج و بهبود آرتریت روماتوئید (بروس-کلر و همکاران ، 1999 ؛ هارتمن و همکاران ، 2012 ؛ مولر و همکاران ، 2001). همانطور که در ادامه این مقاله به تفصیل آورده شده است ، یافته های تحقیقات به خوبی کنترل شده در حیوانات آزمایشی و یافته های جدید از انسان
درسهای ساده Oرژیمها
اثرات چشمگیر CR 20-40٪ معمول در پیری و بیماریها در موش و موش صحرایی اغلب به عنوان پاسخهای تکامل یافته در پستانداران برای انطباق با دوره های دسترسی محدود به غذا مشاهده می شود (Fontana and Klein، 2007؛ Fontana et al.، 2010؛ ماسورو ، 2005 ؛ ویندروخ و والفورد ، 1988). با این حال ، مکانیسم های سلولی و مولکولی مسئول اثرات محافظتی CR میلیاردها سال پیش در تلاش برای زنده ماندن پروکاریوت ها در محیطی کاملاً یا کاملاً فاقد منابع انرژی تکامل یافته اند در حالی که از آسیب وابسته به سن که می تواند تناسب اندام را به خطر بیاندازد ، جلوگیری می کنند. در واقع ، E. coli از a تغییر حالت داد
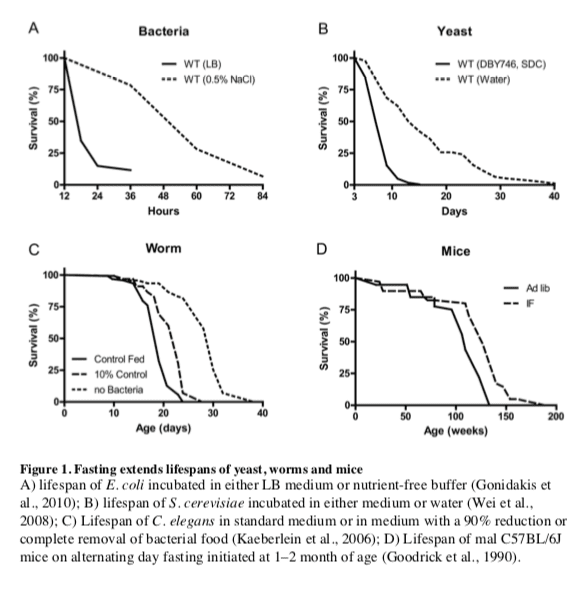
در مخمر S. cerevisiae، سلول های سوئیچینگ از محیط رشد استاندارد به آب همچنین باعث افزایش طول عمر طولانی مدت 2 و همچنین افزایش قابل توجهی در مقاومت در برابر تنش های متعدد (شکل 1B) (Longo و همکاران، 1997، Longo و غیره، 2012). مکانیسم های طول عمر وابسته به محرومیت از مواد غذایی شامل تنظیم پایین تر از پاسخ اسید آمینه Tor-S6K (Sch9) مسیر و همچنین از
یکی دیگر از ارگانیسم های مدل بزرگ که در آن روزه طول عمر طول می کشد نماتد C.
در مگس، بیشتر مطالعات نشان می دهد که محرومیت مکرر مواد غذایی طول عمر را تحت تاثیر قرار نمی دهد (Grandison et al.، 2009). با این وجود، کاهش غذا یا رژیم غذایی به طور پیوسته نشان داده شده است که طول عمر Drosophila را افزایش دهد (Piper and Partridge، 2007) که نشان می دهد مگس ها می توانند از محدودیت غذا بهره مند شوند، اما ممکن است حساس به دوره های گرسنگی حتی کوتاه باشند.
با هم این نتایج نشان می دهد که محرومیت از مواد غذایی می تواند اثرات طول عمر را در انواع مختلف ارگانیسم ها منجر شود، بلکه تأکید می کند که ارگانیسم های مختلف پاسخ های مختلفی به روزه دارند.
پاسخ های سازگار به روزه در مammals
در اکثر پستانداران، کبد به عنوان مخزن اصلی گلوکز عمل می کند که به شکل گلیکوژن ذخیره می شود. در انسان، بسته به فعالیت بدنی آنها، ساعتهای ناشی از 12 به 24 به طور معمول باعث کاهش 20٪ یا بیشتر در گلوکز سرم و کاهش گلیکوژن درون کبدی می شود، همراه با تغییر در متابولیسم
روزه و مغز
در پستانداران، محرومیت شدید CR / مواد غذایی باعث کاهش اندازه بسیاری از اندامها به جز مغز و بیضه ها در موش های نر (Weindruch and Sohal، 1997) می شود. از یک تکامل
به خصوص با توجه به پاسخ های انطباقی مغز به دسترسی محدود به مواد غذایی در طول تکامل انسان جالب است
گرسنگی یک واکنش تطبیقی برای محرومیت از مواد غذایی است که شامل تغییرات حسی، شناختی و عصبی عضلانی است که انگیزه دادن و فعال کردن رفتارهای غذا را ایجاد می کنند. پیشنهاد شده است که شبکه های عصبی مرتبط با گرسنگی، neuropeptides
روزه، پیری و بیماری در گاو نرکوئلز
روش های مختلف روزه گیری و پیری
تفاوت عمده بین IF و PF در موش ها طول و فرکانس چرخه های سریع است. چرخه های عادی معمولا ساعت های 24 را طی می کنند و یک تا چند روز از هم جدا می شوند، در حالی که دوره های PF 2 یا بیشتر روزها را می گذرانند و حداقل از 1 جدا نیستند، که برای موش ضروری است تا وزن طبیعی خود را دوباره به دست آورند. یک تفاوت در تغییرات مولکولی ناشی از رژیمهای گوناگون ناشتا، تأثیر آن بر عوامل مختلف رشد و نشانگرهای متابولیکی است که IF باعث تغییرات مکرر اما کمتر از PF می شود. مهم است که تعیین کنیم که چگونه فرکانس تغییرات خاص مانند کاهش IGF-1 و گلوکز بر تأثیر سلول، بیماری ها
روزه و سیancer
روزه می تواند اثرات مثبت داشته باشد
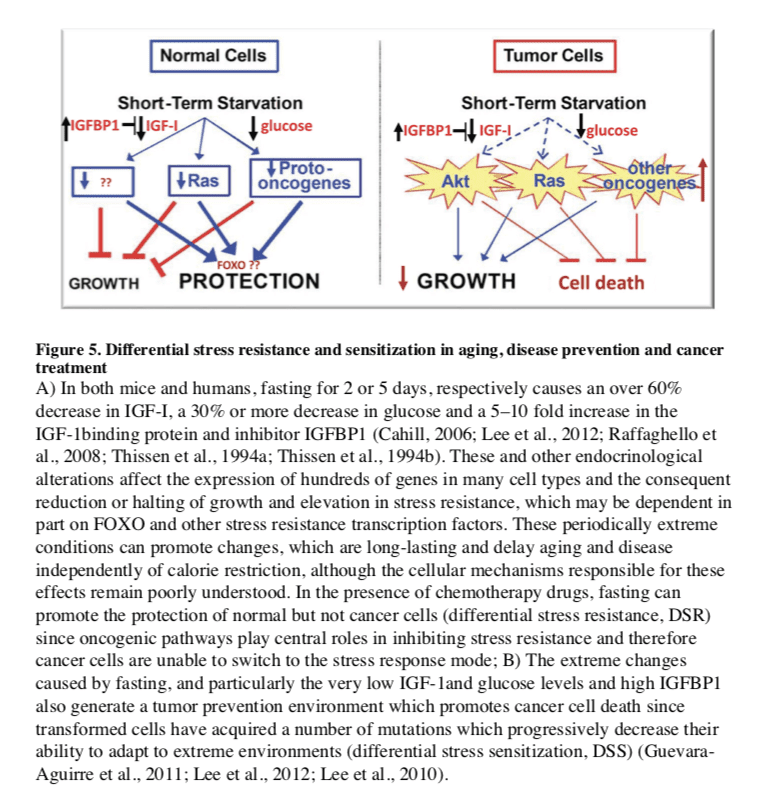
در درمان سرطان نشان داده شده است که روزه داری اثرات مثبت و منسجم تری دارد. نشان داده شد كه PF به مدت 2 to3 روز از موشها در برابر انواع داروهای شیمی درمانی محافظت می كند ، تاثیری به نام مقاومت استرس افتراقی (DSR) برای انعكاس عدم توانایی محافظت سلولهای سرطانی بر اساس نقش انكوژنها در تنظیم منفی مقاومت به استرس ، بنابراین ارائه سلولهای سرطانی ، در تعریف ، قادر به محافظت در برابر شرایط روزه داری نیستند (شکل 5) (Raffaghello و همکاران ، 2008). PF همچنین باعث حساسیت عمده سلولهای مختلف سرطانی در درمان شیمیایی می شود ، زیرا باعث ایجاد یک محیط فوق العاده در ترکیب با شرایط استرس ناشی از شیمی درمانی می شود. بر خلاف حالت محافظت شده توسط سلولهای طبیعی در هنگام روزه داری ، سلولهای سرطانی قادر به سازگاری نیستند ، پدیده ای به نام حساسیت استرس افتراقی (DSS) ، بر اساس این تصور که اکثر جهش ها مضر هستند و بسیاری از جهش های جمع شده در سلول های سرطانی باعث رشد می شوند در شرایط استاندارد اما آنها را در سازگاری با محیطهای شدید بسیار کم می کند (لی و همکاران ، 2012). در مدل های موش از تومورهای متاستاتیک ، ترکیبی از روزه داری و شیمی درمانی که باعث DSR و DSS می شود ، منجر به زنده ماندن بدون سرطان 20 تا 60٪ در مقایسه با همان سطح شیمی درمانی یا روزه داری به تنهایی می شود ، که برای ایجاد بقای بدون سرطان کافی نیست (لی و همکاران ، 2012 ؛ شی و همکاران ، 2012). بنابراین ، این ایده که سرطان تنها با هفته ها روزه داری قابل درمان است ، دهه ها پیش رایج شد ،
روزه و نایجاد یورو
در مقایسه با گروه کنترل با تغذیه آزاد ، موش ها و موش هایی که تحت رژیم IF قرار دارند ، عملکرد عصبی و انحطاط عصبی کمتری دارند و علائم بالینی کمتری در مدل های بیماری آلزایمر (AD) ، پارکینسون (PD) و بیماری هانتینگتون نشان می دهند. (HD) این مدلها شامل موشهای تراریخته هستند که ژنهای انسانی جهش یافته را بیان می کنند که باعث AD موروثی غالب (پروتئین پیش ساز آمیلوئید و پرزنیلین -1) و زوال عقل لوب جلوی تمپورال (Tau) (Halagappa و همکاران ، 2007) ، PD (؟ -سینوکلئین) (Griffioen و همکاران) می شود. ، 2012) و HD (هانتینگتین) (دوان و همکاران ، 2003) ، و همچنین مدلهای مبتنی بر نوروتوکسین مربوط به AD ، PD و HD (بروس-کلر و همکاران ، 1999 ؛ دوان و ماتسون ، 1999). حیواناتی که تحت رژیم IF هستند نیز پس از آسیب حاد از جمله تشنج شدید صرع ، سکته مغزی و آسیب های مغزی و نخاعی آسیب دیده ، بهتر از کنترل های تغذیه شده آزاد (Arumugam و همکاران ، 2010 ؛ بروس-کلر و دیگران ، 1999 ؛ Plunet و al. ، 2008).
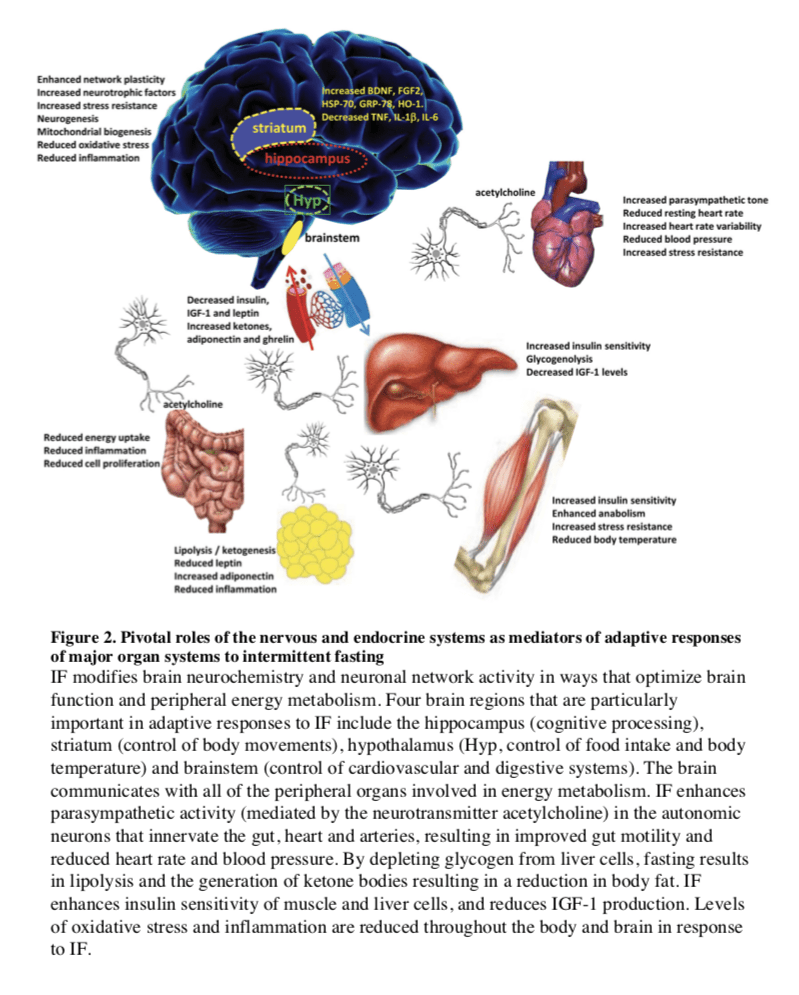
چندین مکانیسم سلولی وابسته به اثرات مفید IF در سیستم عصبی از جمله کاهش تجمع مولکول های آسیب دیده اکسیداتیو، بهبود زیست فعال انرژی سلولی، افزایش سیگنال های عامل نوروئیدی و کاهش التهاب (Mattson، 2012a) کمک می کند. مکانیسم های محافظتی عصبی اخیر توسط مطالعات نشان داده شده است که رژیم های غذایی IF باعث افزایش سطوح دفاع از آنتی اکسیدان، عوامل نوروئیدی (BDNF و FGF2) و پروتئین شاپرن ها (HSP-70 و GRP-78) و کاهش سطح
روزه و متابولیک Sیندرم
سندرم متابولیک (MS) که به عنوان چربی شکم تعریف شده است، همراه با مقاومت به انسولین، افزایش تری گلیسیرید و / یا فشار خون بالا، خطر بیماری قلبی عروقی، دیابت، سکته مغزی را به میزان قابل توجهی افزایش می دهد
تغییرات هورمونی متعددی که MS را در انسان نشان می دهد a

رژیم تقلید روزه ProLon یک برنامه 5 روزه است که شامل مواد طبیعی توسعه یافته و آزمایش شده بالینی است که بدن انسان را به حالت روزه "فریب" می دهد. FMD دارای کربوهیدرات و همچنین پروتئین کم و چربی زیادی است. رژیم تقلیدی روزه دار ProLon مزایای مختلف سلامتی را شامل می شود ، از جمله کاهش وزن و کاهش چربی شکم ، همه در حالی که توده بدن سرب را حفظ می کند ، سطح انرژی را بهبود می بخشد ، پوست نرم تر و سالم تر ، و همچنین سلامت و سلامتی کلی را حفظ می کند.
دکتر الکس جیمنز DC، CCST InsightFMD می تواند طول عمر را افزایش دهد.
روزه، پیری و بیماری در هumans
روزه و عوامل موثر در پیری
داده های بالینی و اپیدمیولوژیک سازگار است
از جمله اثرات مهم روزه دار مربوط به پیری و بیماری ها است
اگر دوره تغذیه بیش از حد افراد در نظر گرفته شود ، می توان با کمترین میزان کالری دریافتی به دست آورد. بنابراین ، چرخه های روزه داری یک استراتژی بسیار عملی تر برای دستیابی به اثرات مفید CR و احتمالاً اثرات قوی تر ، بدون بار کمبود تغذیه مزمن و برخی از اثرات سو provide بالقوه مرتبط با کاهش وزن یا BMI بسیار کم ، فراهم می کند. در حقیقت ، افراد دارای اضافه وزن متوسط (BMI 25-30)) در زندگی بعدی می توانند خطر مرگ و میر کلی را در مقایسه با افراد با وزن طبیعی کاهش دهند (Flegal و همکاران ، 2013). اگرچه این نتایج ممکن است تحت تأثیر وجود بسیاری از آسیب شناسی های موجود یا در حال توسعه در گروه کنترل وزن کم باشد ، اما بر ضرورت تمایز بین افراد جوان و افراد مسنی که ممکن است از CR یا روزه داری برای کاهش وزن یا تأخیر در پیری استفاده کنند ، تأکید می کنند. اگرچه مداخلات رژیم غذایی شدید در دوران پیری ممکن است در برابر بیماری های مربوط به سن محافظت کند ، اما این می تواند اثرات مخربی بر روی سیستم ایمنی بدن و توانایی پاسخ به برخی از بیماری های عفونی ، زخم ها و چالش های دیگر داشته باشد (کریستان ، 2008 ؛ رید و همکاران ، 1996) با این حال ، IF یا PF که برای جلوگیری از کاهش وزن و به حداکثر رساندن تغذیه طراحی شده است ، می تواند اثرات مفیدی روی بیماری های عفونی ، زخم ها داشته باشد.
روزه و سیancer
روزه داری برای پیشگیری و درمان سرطان بالقوه است. اگر چه هیچ اطلاعات انسانی بر روی تاثیر IF یا PF در پیشگیری از سرطان در دسترس نیست، اما تاثیر آن بر کاهش سطح IGF-1، انسولین و گلوکز، و افزایش سطح IGFBP1 و کتون بدن می تواند یک محیط محافظ ایجاد کند که آسیب DNA و سرطان زایی را کاهش دهد، در حالی که در عین حال ایجاد شرایط خصمانه برای سلول های تومور و پیش سرطانی (شکل 5). در واقع، افزایش گردش خون IGF-1 با افزایش خطر ابتلا به سرطان های خاص (Chan و همکاران، 2000، Giovannucci و همکاران، 2000) و افراد مبتلا به کمبود IGF-1 شدید ناشی از کمبود گیرنده هورمون رشد، به ندرت سرطان ( Guevara-Aguirre و همکاران، 2011، Shevah و Laron، 2007، Steuerman و دیگران، 2011). علاوه بر این، سرم از این افراد IGF-1deficient محافظت از سلول های اپیتلیال انسان از آسیب DNA ناشی از استرس اکسیداتیو. علاوه بر این، زمانی که DNA آنها آسیب دیده بود، سلول ها احتمال بیشتری برای مرگ سلول های برنامه ریزی شده داشتند (Guevara-Aguirre et al.، 2011). بنابراین، روزه می تواند از طریق کاهش آسیب سلولی و DNA و همچنین افزایش مرگ سلول های پیش سرطانی از سرطان محافظت کند.
در یک مطالعه اولیه از افراد 10 با انواع بدخیمی، ترکیب شیمی درمانی با روزه موجب کاهش در تعدادی از عوارض جانبی معمول خود ناشی از شیمی درمانی در مقایسه با افراد مشابه که تحت شیمی درمانی در حالی که در یک رژیم غذایی استاندارد (Safdie و غیره، 2009). تأثیر روزه داری بر سمیت شیمی درمانی و پیشرفت سرطان در حال حاضر در آزمایشات بالینی در اروپا و ایالات متحده آمریکا (0S-08-9، 0S-10-3) آزمایش می شود.
روزه و نایجاد یورو
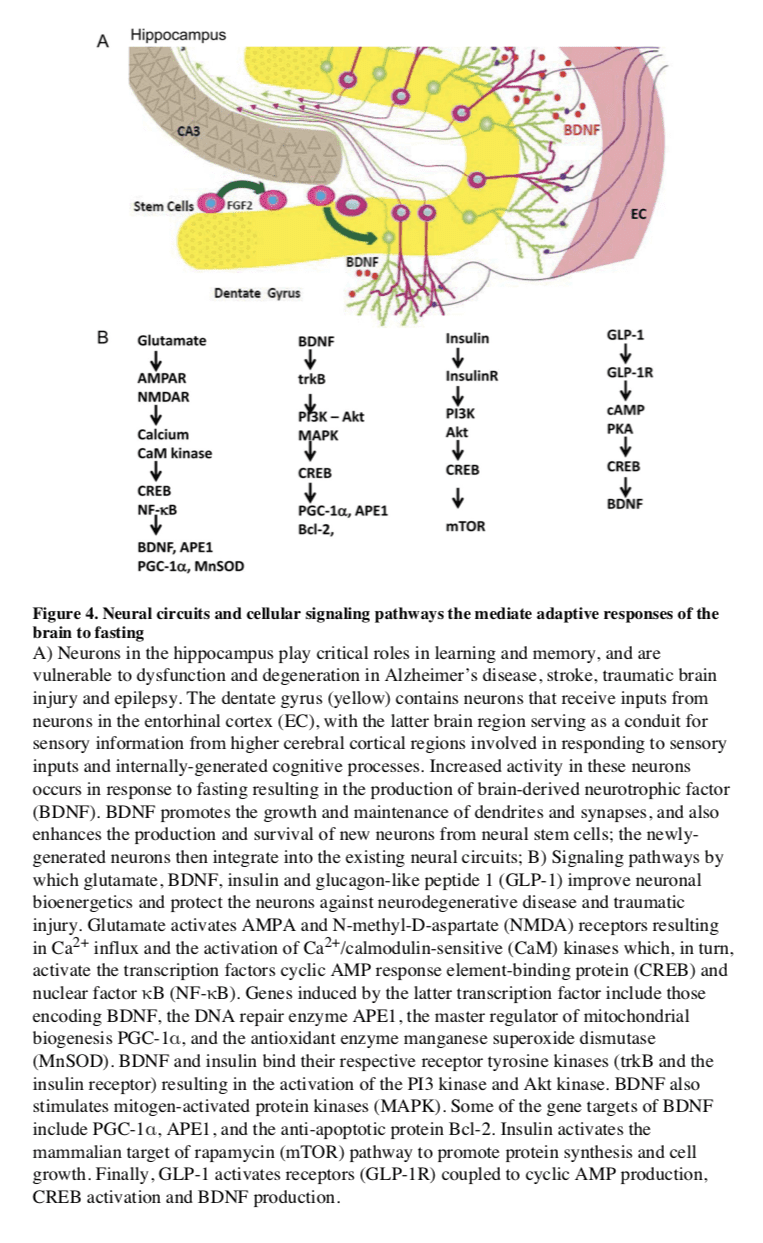
درک کنونی ما در مورد تأثیر IF در سیستم عصبی و عملکرد شناختی عمدتا از مطالعات حیوانی (به بالا) اشاره می شود. مطالعات مداخله ای برای تعیین تأثیر روزه داری بر عملکرد مغز و فرآیندهای بیماری های عصبی مصنوعی وجود ندارد.
پس از 3 4 ماه ، CR عملکرد شناختی (حافظه کلامی) را در زنان دارای اضافه وزن بهبود بخشید (کرچ و همکاران ، 1997) و در افراد مسن (ویت و همکاران ، 2009). به طور مشابه ، هنگامی که افراد با اختلال شناختی خفیف به مدت 1 ماه با رژیم کم قند خون حفظ شدند ، آنها حافظه بینایی تاخیری بهبود یافته ، نشانگرهای زیستی مایع مغزی نخاعی را نشان دادند؟ متابولیسم و انرژی زیستی مغز (Bayer-Carter et al.، 2011). مطالعاتی که در آن عملکرد شناختی ، حجم منطقه ای مغز ، فعالیت شبکه عصبی و تجزیه و تحلیل بیوشیمیایی مایع مغزی نخاعی در افراد انسانی قبل و در طی یک دوره طولانی IF اندازه گیری می شود ، باید تأثیر IF بر ساختار مغز و عملکرد انسان را روشن کند.
روزه، التهاب و Hفشار خون بالا
در انسان ، یکی از بهترین تأثیرات مفید روزه داری طولانی مدت به مدت یک تا 3 هفته در درمان آرتریت روماتوئید (RA) است. در توافق با نتایج حاصل از جوندگان ، شکی نیست که در طول روزه داری ، هم التهاب و هم درد در بیماران RA کاهش می یابد (مولر و همکاران ، 2001). با این حال ، پس از شروع رژیم غذایی طبیعی ، التهاب برمی گردد مگر اینکه دوره ناشتایی با رژیم گیاهخواری دنبال شود (Kjeldsen-Kragh و همکاران ، 1991) ، یک درمان ترکیبی که دارای اثرات مفید برای دو سال یا بیشتر است (Kjeldsen-Kragh et همکاران ، 1994) روایی این روش توسط چهار مطالعه کنترل شده متفاوت ، از جمله دو کارآزمایی تصادفی ، پشتیبانی می شود (مولر و همکاران ، 2001). بنابراین ، روزه داری همراه با رژیم گیاهخواری و احتمالاً با سایر رژیم های غذایی اصلاح شده اثرات مفیدی در درمان RA دارد. اگر روز متناوب نیز منجر به کاهش قابل توجهی در TNF سرم شود؟ و سرامیدها در بیماران آسم طی یک دوره 2 ماهه (جانسون و همکاران ، 2007). مطالعه اخیر بیشتر نشان داد که نشانگرهای استرس اکسیداتیو که اغلب با التهاب (پروتئین و اکسیداسیون لیپید) همراه هستند ، در پاسخ به IF به طور قابل توجهی کاهش می یابد. بنابراین ، برای بسیاری از بیمارانی که قادر به تحمل روزه داری طولانی مدت و تغییر دائمی در رژیم غذایی خود هستند ، دوره های روزه داری نه تنها باعث تقویت بلکه جایگزین درمان های پزشکی موجود می شوند.
تنها آب و سایر اشکال ناشی از طولانی مدت نیز برای تأثیرات شدید در فشار خون بالا ثبت شده است. به طور متوسط روزانه 13 آب تنها ناشتا منجر به دستیابی به
برای هر دو فشار خون بالا و
روزه و متابولیک Sیندرم
روزهدار دوره ای می تواند چندین ویژگی سندرم متابولیک در انسان را معکوس کند: حساسیت انسولین را افزایش می دهد، لیپولیز را تحریک می کند و فشار خون را کاهش می دهد. چربی بدن و فشار خون کاهش می یابد و متابولیسم گلوکز در افراد چاق در پاسخ به روزهای متناوب روزه بهبود یافته است (Klempel et al.، 2013؛ Varady et al.، 2009). افراد دارای اضافه وزن برای ماه 6 در سال

نتیجه گیری و توصیه
بر اساس شواهد موجود در مطالعات حیوانی و انسانی شرح داده شده است، ما نتیجه می گیریم که پتانسیل زیادی برای شیوه زندگی وجود دارد که روزه های دوره ای را در طول زندگی بزرگسالان به وجود می آورد تا سلامت مطلوب را ارتقا دهد و خطر بسیاری از بیماری های مزمن را کاهش دهد، به ویژه برای افرادی که اضافه وزن دارند. مطالعات حیوانی اثرات قوی و تکراری ناشتا را در شاخص های سلامت شامل حساسیت به انسولین بیشتر و کاهش فشار خون، چربی بدن، IGF-I، انسولین، گلوکز، لیپید های آتروژنیک و التهاب گزارش داده اند. رژیم های روزانه می توانند فرآیندهای بیماری را بهبود بخشند و نتایج عملکردی را در مدل های حیوانی اختلالاتی که شامل انفارکتوس میوکارد، دیابت، سکته مغزی، AD و PD هستند را بهبود بخشد. یکی از مکانیسم های عمومی روزه داری این است که پاسخ های استرس انطباقی را به وجود می آورد که منجر به افزایش توانایی برای مقابله با استرس شدید و مقابله با بیماری ها می شود. علاوه بر این، از طریق محافظت از سلول ها از آسیب DNA، سرکوب رشد سلول و افزایش آپوپتوز سلول های آسیب دیده، ناشتا می تواند مانع تشکیل و رشد سرطان ها شود.
با این حال ، مطالعات مربوط به رژیم های روزه داری در کودکان ، افراد بسیار مسن و کم وزن انجام نشده است و این احتمال وجود دارد که IF و PF برای این جمعیت مضر باشد. دوره های ناشتایی بیش از 24 ساعت و به ویژه آنهایی که 3 روز یا بیشتر طول می کشد باید تحت نظارت پزشک و ترجیحاً در کلینیک انجام شود. رویکردهای مبتنی بر IF و PF برای مقابله با اپیدمی های فعلی اضافه وزن ، دیابت و بیماری های مربوطه باید در مطالعات تحقیقات انسانی و برنامه های درمانی پزشکی دنبال شود. چندین نسخه از "نسخه های سریع" بالقوه که برای افراد دارای اضافه وزن استفاده شده اند ، حول موضوع مشترک پرهیز از مصرف غذا و نوشیدنی های کالری حداقل به مدت 12 24 ساعت در یک یا چند روز در هفته یا ماه ، بسته به طول ترکیب ، با ورزش منظم. برای افرادی که دارای اضافه وزن هستند ، پزشکان می توانند از بیماران خود بخواهند مداخله روزه داری را انتخاب کنند که به اعتقاد آنها براساس برنامه روزانه و هفتگی آنها می توانند آن را رعایت کنند. بعنوان مثال می توان به رژیم 5: 2 IF (هاروی و همکاران ، 2011) ، رژیم ناشتا اصلاح شده روزانه (جانسون و همکاران ، 2007 ؛ وارادی و همکاران ، 2009) ، 4 5 روز سریع یا کم کالری اشاره کرد. اما رژیم های غذایی ناشتا با تغذیه زیاد هر 1 3 ماه یک بار و به دنبال آن در صورت لزوم هر روز یک وعده اصلی را حذف کنید (V. Longo ، آزمایش بالینی در حال انجام است). یکی از نگرانی های رژیم های متناوب نامتعادل مانند رژیم هایی که در آنها دریافت کالری کم فقط به مدت 2 روز در هفته مشاهده می شود ، تأثیرات بالقوه بر ریتم شبانه روزی و سیستم غدد درون ریز و دستگاه گوارش است که تحت تأثیر عادات غذایی شناخته می شوند. در طول 4 6 هفته اول اجرای رژیم ناشتا ، یک پزشک یا یک متخصص تغذیه ثبت شده باید بطور منظم با بیمار در تماس باشد تا روند پیشرفت وی را کنترل کند و مشاوره و نظارت را ارائه دهد.
رژیم های ناشتا همچنین می تواند برای بیماری های خاص به عنوان درمان های مستقل یا کمکی تنظیم شود. نتایج آزمایشات اولیه IF (روزه گرفتن 2 روز در هفته یا یک روز در میان) در افراد انسانی حاکی از آن است که یک دوره گذار انتقالی 3 6 هفته وجود دارد که طی آن مغز و بدن با الگوی غذایی جدید سازگار می شوند و روحیه افزایش می یابد (هاروی و همکاران ، 2011 ؛ جانسون و همکاران ، 2007). اگرچه حدس و گمان است ، اما به احتمال زیاد در دوره انتقال اخیر ، نوروشیمی مغز تغییر کند تا "اعتیاد" به مصرف منظم غذا در طول روز برطرف شود. قابل توجه است ، رویکردهای مختلف روزه داری احتمالاً به ویژه در افزایش سن و سایر شرایط به غیر از چاقی ، اثر محدودی دارند مگر اینکه با رژیم های غذایی مانند کالری دریافتی متوسط و رژیم های غذایی کم پروتئین مدیترانه ای یا اوکیناوا (0.8 گرم پروتئین / کیلوگرم وزن بدن) ترکیب شوند. ) ، به طور مداوم با سلامتی و طول عمر همراه است.
در آینده، مهم است که ترکیب داده های اپیدمیولوژیک، مطالعات جمعیت های طولانی مدت و رژیم های غذایی آنها، نتایج ارگانیسم های مدل که مولفه های خاصی از رژیم غذایی را به عوامل پیری و فاکتور پرولاسیک متصل می کنند، با داده های مطالعه ای در مورد رژیم های ناشتا در انسان ، برای طراحی مطالعات بالینی بزرگ که روزه داری را با رژیم های غذایی که به عنوان محافظ و لذت بخش شناخته می شوند ادغام می کنند. درک بهتر مکانیسم های مولکولی که روزه داری بر انواع مختلف سلول ها و سیستم های عضو تاثیر می گذارد، باید منجر به ایجاد مداخلات پیشگیرانه و درمانی جدید برای طیف گسترده ای از اختلالات شود.
گرفتن پیغام خانگی
رژیم غذایی روزه داری، با محدود کردن مصرف کالری شما برای مدت پنج روز از ماه، به جای آنکه به طور کامل چندین روز یا حتی هفته ها را تمام مواد غذایی را از بین ببرد، مزایای روزانه سنتی را نیز دارد. این ProLon رژیم غذایی روزمره یک برنامه غذای روزانه 5 ارائه می دهد که به صورت جداگانه بسته بندی و برچسب گذاری شده در مقادیر و ترکیبات دقیق برای هر روز است. اگر چه مطالعات انجام شده در بالا مزایای سلامت ناشتا را نشان می دهد، لطفا قبل از شروع به صحبت با متخصص مراقبت های بهداشتی رژیم تقلید روزه ProLon ، برنامه 5 روزه وعده غذایی برای پیدا کردن اگر FMD، و یا هر رژیم غذایی دیگری، برای شما مناسب است.
فرم منتشر شده، نهایی ویرایش شده از مطالعه تحقیقاتی که در بالا ذکر شد، در دسترس قرار گرفت دسترسی به دسترسی عمومی NIH دست خط در PMC فوریه 4، 2015. محدوده اطلاعات ما محدود به مسائل مربوط به مراقبت از کراپراککت، نخاع و موضوعات پزشکی کاربردی است. برای بحث در مورد موضوع، لطفا از دکتر الکس جیمنز سوال کنید یا با ما تماس بگیرید 915-850-0900 .
دکتر الکس جیمنز سرپرستی می کند
اشاره از: Nih.gov

بحث در مورد مبحث اضافی: درد حاد کمر
درد پشت یکی از شایع ترین علل ناتوانی و از دست رفتن روز در کار در سراسر جهان است. درد پشت به دومین علت رایج در بازدید پزشکان پزشکی مربوط می شود، که تنها توسط عفونت های تنفسی فوقانی می شود. تقریبا 80 درصد از جمعیت حداقل یک بار در طول زندگی خود درد زایمان را تجربه خواهند کرد. ستون فقرات شما یک ساختار پیچیده است که از استخوان ها، مفاصل، رباط ها و عضلات در میان دیگر بافت های نرم تشکیل شده است. آسیب و / یا شرایط سخت، مانند دیسک های فتق دیسک، در نهایت می تواند منجر به علائم درد پشت شود. آسیب های ورزشی یا آسیب های ناشی از تصادفات خودرو اغلب اغلب علت درد پشت هستند، اما گاهی اوقات ساده ترین حرکات می توانند نتایج دردناکی داشته باشند. خوشبختانه، گزینه های درمان جایگزین، مانند مراقبت از کیهان پراکسی، می تواند به کاهش درد در استفاده از تنظیمات ستون فقرات و دستکاری دست کمک کند و در نهایت بهبود تسکین درد را کاهش دهد.
XYMOGEN فرمول های حرفه ای منحصر به فرد از طریق انتخاب مجوز متخصصان مراقبت های بهداشتی در دسترس هستند. فروش اینترنتی و تخفیف فرمول های XYMOGEN به شدت ممنوع است.
با افتخار، دکتر الکساندر جیمنز فرمولهای XYMOGEN را فقط برای بیماران تحت مراقبت خود در دسترس قرار می دهیم.
لطفا به دفتر ما تماس بگیرید تا ما بتوانیم مشاوره دکتر را برای دسترسی سریع اختصاص دهیم.
اگر بیمار هستید کلینیک پزشکی و عمل جراحی آسیب، ممکن است در مورد XYMOGEN با فراخوانی سوال کنید 915-850-0900.
برای راحتی شما و بررسی از XYMOGEN محصولات لطفا لینک زیر را بررسی کنید. *XYMOGEN-Catalog-دانلود
* تمامی خط مشی های XYMOGEN بالا به شدت تحت فشار هستند.
***
اطلاعات اینجا در "رژیم غذایی تقلید روزانه توضیح داده شده است"در نظر گرفته شده است که جایگزین رابطه یک به یک با یک متخصص مراقبت های بهداشتی واجد شرایط یا پزشک دارای مجوز نیست و توصیه پزشکی نیست. ما شما را تشویق می کنیم که تصمیمات مراقبت های بهداشتی را بر اساس تحقیقات و مشارکت خود با یک متخصص مراقبت های بهداشتی واجد شرایط اتخاذ کنید.
محدوده اطلاعاتی ما محدود به کایروپراکتیک، اسکلتی عضلانی، داروهای فیزیکی، سلامتی، کمک کننده به علت اختلالات احشایی در ارائه های بالینی، پویایی بالینی رفلکس سوماتوویسرال مرتبط، کمپلکس های سابلوکساسیون، مسائل حساس سلامتی، و/یا مقالات، موضوعات و بحث های پزشکی کاربردی.
ارائه و ارائه می کنیم همکاری بالینی با متخصصین رشته های مختلف هر متخصص بر اساس حوزه فعالیت حرفه ای و صلاحیت مجوز آنها اداره می شود. ما از پروتکل های عملکردی سلامت و تندرستی برای درمان و حمایت از مراقبت از آسیب ها یا اختلالات سیستم اسکلتی عضلانی استفاده می کنیم.
ویدیوها، پستها، موضوعات، موضوعات و بینشهای ما، موضوعات، مسائل و موضوعات بالینی را پوشش میدهد که به طور مستقیم یا غیرمستقیم به حوزه عمل بالینی ما مربوط میشود و به طور مستقیم یا غیرمستقیم از آن پشتیبانی میکند.*
دفتر ما به طور منطقی تلاش کرده است تا استنادات حمایتی ارائه دهد و مطالعه تحقیقاتی یا مطالعات مرتبط با پست های ما را شناسایی کرده است. ما کپی از مطالعات تحقیقاتی پشتیبانی را که در صورت درخواست در دسترس هیئت های نظارت و عموم است ، ارائه می دهیم.
ما می فهمیم که مواردی را پوشش می دهیم که نیاز به توضیح اضافی در مورد چگونگی کمک به آن در یک برنامه مراقبت خاص یا پروتکل درمانی دارند. بنابراین ، برای بحث بیشتر در مورد موضوع فوق ، لطفاً آزادانه س .ال کنید دکتر الکس جیمنز، دی سی, و یا با ما تماس بگیرید در 915-850-0900.
ما برای کمک به شما و خانواده شما اینجا هستیم.
نعمت
دکتر الکس جیمنز DC ، MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
ایمیل شما: coach@elpasofunctionalmedicine.com
دارای مجوز به عنوان دکتر کایروپراکتیک (DC) در وابسته به تکزاس & نیومکزیکو*
مجوز تگزاس دی سی شماره TX5807, نیومکزیکو دی سی مجوز # NM-DC2182
دارای مجوز به عنوان پرستار ثبت شده (RN*) in فلوریدا
مجوز RN مجوز فلوریدا # RN9617241 (شماره کنترل 3558029)
وضعیت فشرده: مجوز چند ایالتی: مجاز به تمرین در کشورهای 40*
دکتر الکس جیمنز DC، MSACP، RN* CIFM*، IFMCP*، ATN*، CCST
کارت ویزیت دیجیتال من









